
题目列表(包括答案和解析)
15.某溶液中由水电离出的H+浓度为1×10-14mol/L,在此溶液中可能大量共存的离子是
A.Cl-、NO3-、Fe2+、Al3+ B.K+、Fe2+、Cl-、MnO4-
C.K+、AlO2-、Na+、OH- D.Na+、K+、NO3-、HCO3-
14.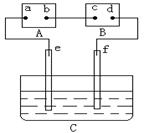 下图中A为电源B为浸透饱和食盐水和酚酞试液的滤纸C为盛有稀硫酸的电解槽,e、f为Pt电极。接通电源后,发现d点显红色。下列有关说法正确的是
下图中A为电源B为浸透饱和食盐水和酚酞试液的滤纸C为盛有稀硫酸的电解槽,e、f为Pt电极。接通电源后,发现d点显红色。下列有关说法正确的是
A.电源A上的a极是正极
B.d极上的电极反应方程式为2Cl--2e-=Cl2↑
C.e、f极上产生的气体体积比为2:1
D.C中溶液的pH增大
13.在盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电一定时间后
A.溶液的PH将增大 B.溶液中的钠离子与碳酸根离子的数目不变
C.溶液的浓度增大并有晶体析出 D. 溶液的浓度不变并有晶体析出
12.电解100mL含c(H+) = 0.30 mol•L-1的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是
A. 0.10 mol•L-1Ag+ B. 0.20 mol•L-1 Zn2+
C. 0.20 mol•L-1 Cu2+ D. 0.20 mol•L-1 Pb2+
11.25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
A.c(NH4+)<c(SO42-) B.2c(NH4+)=c(SO42-)
C.c(NH4+)>c(SO42-) D.c(OH-)+c(SO42-) = c(NH4+)+c(H+)
10.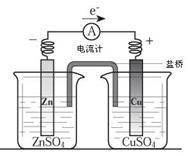 关于如图所示装置的叙述,正确的是
关于如图所示装置的叙述,正确的是
A.铜是阳极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
9.将足量BaCO3粉末分别加入下列溶液中,充分溶解至溶液饱和。各溶液中Ba2+的浓度最小的为:
A.40mL 水 B.10mL 0.2mol/LNa2CO3溶液
C.50mL 0.01mol/L 氯化钡溶液 D.100mL 0.01mol/L盐酸
8. 将Al片和Cu片用导线联接,一组插入浓硝酸中,一组插入稀氢氧化钠溶液中,分别形成的原电池,在这两个原电池中,负极分别为
A.Cu片、Al片 B. Al片、Cu片 C.Al片、Al片 D.Cu片、Cu片
7.下列物质水解的离子方程式书写正确的是
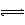 A.NH4NO3 NH4+ + H2O NH3 + H2O
+ H+
A.NH4NO3 NH4+ + H2O NH3 + H2O
+ H+
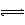 B.CuSO4 Cu2+ + 2H2O Cu(OH)2↓ + 2H+
B.CuSO4 Cu2+ + 2H2O Cu(OH)2↓ + 2H+
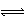 C.Na2CO3 CO32ˉ + 2H2O
H2O + CO2↑+ OH-
C.Na2CO3 CO32ˉ + 2H2O
H2O + CO2↑+ OH-
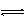 D.KF Fˉ + H2O
HF + OHˉ
D.KF Fˉ + H2O
HF + OHˉ
6.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾为电解质,电池总反应式为Zn(s) + 2MnO2(s) + H2O(l) = Zn(OH)2(s) +Mn2O3(s) 下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e- =Mn2O3(s)+2OH- (aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com