
题目列表(包括答案和解析)
工业上采用________________的方法获得。
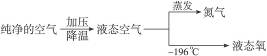
答案:分离液态空气
2.答案:(1)锰酸钾 二氧化锰
(3)气密性 药品 水槽中取出
1.答案:(1)过氧化氢 水 氧气 Ⅰ.木条不复燃 很慢 Ⅱ.有气泡冒出,木条复燃 加快 Ⅲ.木条复燃 加快 没有 质量 化学性质
(2)液体 固体 加热 排水 向上
(3)木条复燃
(4)集气瓶外 集气瓶口
2.在实验室中也可以用高锰酸钾来制取氧气
(1)原理:高锰酸钾 ____________+____________+氧气
____________+____________+氧气
(2)实验装置(发生装置、收集装置):
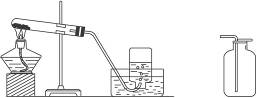
(3)实验室用高锰酸钾制取氧气并用排水法收集的步骤
实验室用高锰酸钾制取氧气并用排水法收集,其步骤可总结为“三先三后”(即先检查装置________________,后装入________________;先预热,后集中在药品的部位加热;先将导管从________________,后熄灭酒精灯),也可缩记为:“查”“装”“定”“点”“收”“离”“熄”,再利用谐音来理解记忆为:茶庄定点收利息。
1.在实验室里可用________________溶液来制取氧气。
(1)原理:(用文字表达式来表示)
过氧化氢 ________________+________________
________________+________________
实验探究二氧化锰的作用:
|
实验编号 |
实验步骤 |
实验现象 |
实验结论 |
|
Ⅰ |
在试管中加入5 mL 5%的过氧化氢溶液,将带火星的木条伸入试管中 |
|
在常温下过氧化氢溶液分解____________ |
|
Ⅱ |
加热上述试管,将带火星的木条伸入试管中 |
|
温度升高,过氧化氢分解速度_________ |
|
Ⅲ |
在另一只试管中加入5 mL 5%的过氧化氢溶液,并加入少量二氧化锰,将带火星的木条伸入试管中 |
|
二氧化锰使过氧化氢分解速度_________ |
若在实验前准确秤出二氧化锰的质量,实验后将二氧化锰回收、干燥、再称量,会发现它的质量____________改变。
结论:二氧化锰可使过氧化氢溶液在常温下迅速分解,作催化剂。
催化剂:在化学反应中能改变反应速率,但本身的____________和____________在反应前后都没有发生变化的物质。
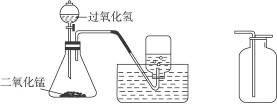
(2)实验装置(发生装置、收集装置)
发生装置的选择:由于过氧化氢是____________,二氧化锰是____________,且反应不需要____________,故采用锥形瓶作为反应容器,配双孔胶塞,一孔插入分液漏斗,另一孔插入导管。
收集装置的选择:由于氧气不易溶于水且不和水反应,故要制取较纯净的气体,需采用____________法。又由于氧气的密度比空气的平均密度大,故要制取较干燥的气体时,需采用____________排空气法。
(3)检验方法
将带火星的木条伸入集气瓶中,如果____________,说明该瓶内的气体是氧气。
(4)验满方法
用排水法收集时,当气泡从____________冒出时,说明该瓶内的气体已满。
用向上排空气法收集时,将带火星的木条放在处,如果木条复燃,说明该瓶内的气体已满。
4.“绿色化学”又称为________,它给化学家提出了一项新的挑战,其核心就是________。
答案:环境友好化学 原子经济论
疑难突破
学习化学有哪些意义?
剖析:(1)可以认识物质变化规律及其性质,弄清生活和生产中的一些现象,可以有效地控制和利用物质的化学变化,造福人类。例如:懂得了燃烧的原理,就可以使燃料充分燃烧,节约能源,并能有效地防火、灭火。
(2)可以使人类更好地认识和利用自然界中的物质,并合成新物质。如利用化学方法,可以将海水淡化,把被污染的水净化后可重新利用,解决人类面临的淡水资源紧缺问题;用电能或太阳能分解水,还可以制得氢气,获得清洁的能源;利用化学可以合成自然界本不存在的、价廉、耐用、抗腐蚀能力强、不易腐烂的塑料等。
(3)应用化学,可促进科学技术的发展,提高人类生活质量。如脱氧核糖核酸结构的发现,打开了分子生物学的大门。化学与生命科学相结合,促进了基因工程的发展,产生了生物克隆技术;利用化学生产化肥和农药,以增加粮食产量;利用化学合成药物,以抑制细菌和病毒,保障人体健康等。
问题探究
问题:怎样学好化学?
探究:学习化学并不难,只要了解学科的特点,注意总结一定的学习方法,就能取得良好的学习效果。这里请同学们注意以下几点:
一是树立信心。化学是中学生必须学好的一门基础自然科学,要充分相信自己的能力,相信自己一定能学好化学。既不能有轻视的思想,更不能有畏难的情绪。
二是加强记忆。初中化学作为起点学科,要认识、了解的新东西太多,如元素符号、元素的化合价、物质的化学式、基本的定义、定律等。要学好化学,记忆是关键,不能仅满足听懂,要在理解的基础上牢固记忆,同时通过练习进一步加深理解。
三是重视实验。化学是一门以实验为基础的学科,要学好化学,必须认真做好实验,仔细观察,并记录和分析实验现象,还要注意联系生活中的化学现象,思考生活中的化学问题。
四是养成良好的思维习惯。思维习惯对于化学学习很重要,对遇到的现象、问题要善于动脑筋,多问几个为什么,并学会对知识的概括和总结,逐渐培养自己分析推理能力,找出学习化学的“窍门”。
五是学好其他学科。学好化学,除要注意化学的学科特点外,更要注意多学科间的渗透与联系。学好数学、物理、生物等是学好化学的有力保证。
典题精讲
例1 著名化学家、诺贝尔化学奖获得者西博格教授在一次报告中讲到:“化学--人类进步的关键”。这句话说明化学与社会、生活、生产和科学技术等方面的联系,指明化学对人类进步起着至关重要作用。试根据你个人的生活经验或查阅资料,举出几例现实生活中应用化学知识的实例:
(1)_______________________________。(2)_______________________________。
(3)_______________________________。(4)_______________________________。
思路解析:本题旨在帮助我们认识化学对人类和社会的重要作用,以培养学习化学的兴趣。通过学习,我们知道,利用化学可生产化肥,农药,合成药物;利用化学可开发新能源和新材料……
答案:(1)食盐是一种调味品 (2)石灰浆刷墙?(3)醋酸除水垢 (4)煤气作燃料等
例2 能源有一级能源和二级能源。自然界以现成形式提供的能源为一级能源;靠其他能源提供能量间接制取的能源为二级能源。下列叙述正确的是( )
A.电能是一级能源 B.天然气是二级能源
C.水力是二级能源 D.酒精(绿色能源)为二级能源
思路解析:本题是一种信息给予迁移应用的题型。要解决这类题目,关键在于利用题目所给的信息分析、判断解决新问题。题中所述一级能源是自然界以现成形式提供的能源,根据这个定义可知,水力、风力、天然气、煤、石油等不需要其他能源制取,是一级能源。而电能是以水力、火力、风力等能源间接制取的;乙醇是以粮食发酵或以石油等物质为原料用工业方法制取的。它们都是二级能源。
答案:D
知识导学
有些物质是由原子构成的,有些物质是由分子构成的。化学反应中发生破裂的是分子,而原子要重新组合,化学反应的本质是原子的重新组合。
门捷列夫发现元素周期表,是化学发展历史上的里程碑。
“绿色化学”的提出,成为化学发展的新阶段。
疑难导析
学习化学的意义要从以下三个方面阐述:
(1)学习化学能否认识物质变化规律及其性质,能否弄清生活和生产中的一些现象,能否有效地控制和利用物质的化学变化,造福人类。可以举燃烧等实例来说明。
(2)学习化学能否使人类更好地认识和利用自然界中的物质,并合成新物质。可以举海水淡化,被污染的水净化,用电能或太阳能分解水,合成自然界本不存在的、价廉、耐用、抗腐蚀能力强、不易腐烂的塑料等实例来说明。
(3)应用化学,能否促进科学技术的发展,提高人类生活质量。可以举脱氧核糖核酸结构的发现、化学与生命科学相结合、利用化学生产化肥和农药、利用化学合成药物等实例来说明。
问题导思
要说明与了解学科的特点、注意总结一定的学习方法间的关系,会取得怎样的学习效果。
要从以下几方面阐述:
一是树立信心与学好化学的关系。
二是加强记忆与学好化学的关系。
三是重视实验与学好化学的关系。
四是养成良好的思维习惯与学好化学的关系。
五是学好其他学科与学好化学的关系。
第一方面要阐述中学生必须学好化学,要树立怎样的信心,要避免什么思想,不要有什么情绪。
第二方面要阐述中学生在初中化学中要了解哪些新东西,学好化学的关键是什么,还要说明听懂、记忆、练习之间的关系。
第三方面要阐述中学生在初中化学学习中怎样做好实验,做实验时要做些什么,要注意哪些问题。
第四方面要阐述对于遇到的现象、问题要怎样做,要学会什么,培养自己什么能力等。
第五方面要阐述为了学好化学,要注意哪些学科特点,对各学科之间的渗透与联系是否也要注意。
典题导考
绿色通道
化学的意义和作用,主要体现在化学对于生活和科技发展的重大促进作用。通过对生活中化学现象的认识和了解,加深对化学学科的理解。培养学习兴趣,有利于促进掌握学习化学的方法。
典题变式
下列说法不正确的是( )
A.化学是人类社会进步的关键
B.学习化学会使你生活得更健康、更文明
C.用化学方法可以合成“长生不老”药
D.使用无硫火柴可减少大气污染
答案:C
绿色通道
这是一道信息给予试题,把握题意是做好该题的基础。对于能源的理解,关键要理解题目中给出的“一级能源和二级能源的根本区别”在于直接来自自然界还是依靠其他能源形式间接获得。
典题变式
(经典回放)“绿色化学”是21世纪化学发展的主导方向。“绿色化学”的目标是在化学产品设计、制造、应用、回收处理时,对环境没有或产生尽可能小的副作用。下列符合“绿色化学”内涵的是( )
A.某冶炼厂将尾气直接排放到空气中
B.执法部门将收缴的假冒伪劣产品焚烧
C.使用含磷洗衣粉
D.开发新型燃氢汽车
答案:D
3.1869年,门捷列夫发现了________和________,使化学学习和研究变得有规律可循。
答案:元素周期表 元素周期律
2.到了近代,由于________和________等科学家的研究,得出了一个重要结论:物质是由________和________构成的,________的破裂和________的重新组合是化学变化的基础。这就是说,在化学变化中,________会破裂,而________不会破裂,但是可重新组合成新的________。________和________的创立,奠定了近代化学的基础。
答案:道尔顿 阿伏加德罗 原子 分子 分子 原子 分子 原子 分子 原子论 分子学说
1.化学是研究物质的________、________、________及________的科学。
答案:组成 结构 性质 变化规律
2.化合价的规律有哪些?
剖析:(1)在化合物里,氧通常显-2价(因为氧原子最外层有6个电子,易得到 2个电子或使电子对偏向)。氢通常显+1价(因为氢原子外层只有1个电子,易失去或使电子对偏离)。金属元素通常显正价(因为其原子的最外层电子数较少,易失去电子)。非金属元素通常显负价(因为其原子的最外层电子数较多,易得到电子或使电子对偏向)。但在非金属氧化物里,氧显负价,另一种非金属元素显正价(因为氧原子得电子能力很强)。
(2)在化合物里,正、负化合价的代数和为零。
(3)在单质中元素的化合价为零。
(4)有些元素的化合价是可变的。可变的原因是这些元素的原子在不同条件下,既可得电子(或电子对偏向),也可失电子(或电子对偏离),而且得失电子数目可以不同。
(5)某些原子团也表现出一定的化合价。
问题探究
问题 举例说明如何计算化合物中某元素的质量分数?
探究:此类题目计算时,应注意解题格式要规范,“100%”不能丢掉,原子个数要统计准确。
某元素的质量分数= ×100%
×100%
例如:计算NH4NO3中氮元素的质量分数。
 ×100%
×100%
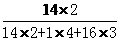 ×100%=35%
×100%=35%
典题精讲
例1 判断下列化学符号中数字“2”的意义,将其序号填在相应的横线上:①Ca2+ ②NO2 ③2NO?④?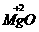 ⑤2
⑤2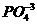
(1)表示分子个数的是__________。
(2)表示一个离子所带电荷数的是__________。
(3)表示元素化合价的是__________。
(4)表示一个分子中所含原子个数的是__________。
思路解析:Ca2+中的“2”表示一个钙离子带两个单位正电荷;NO2中的“2”表示一个NO2分子中含有2个氧原子;2NO中的“2”表示分子个数;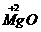 中的“2”表示MgO中Mg元素化合价为+2;2
中的“2”表示MgO中Mg元素化合价为+2;2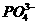 中的“2”表示离子的个数。
中的“2”表示离子的个数。
答案:(1)③ (2)① (3)④ (4)②
例2下列物质含氮量最高的是( )
A.NH4HCO3 B.(NH4)2SO4
C.NH4NO3 D.NaNO3
思路解析:此题有一个巧解法:比较不同物质中含同一元素(或原子团)质量分数的大小时,可以换算成该元素(或原子团)的同一组成的含量,然后比较剩余组成的相对分子质量,根据剩余组成相对分子质量由小到大的顺序,就是对应质量分数由大到小的顺序。
在NH4HCO3中,其余相对式量是H5CO3=65;在(NH4)2SO4中,其余相对式量是H8SO4/2=52;在NH4NO3中,其余相对式量是H4O3/2=26;在NaNO3中,其余相对式量是71。硝酸铵含氮量最高。
答案:C
知识导学
任何纯净物都有固定的组成,一种物质只能有一个化学式。
关于化学式所表达的信息(表示的意义)一定要理解,这对后面的有关化学式的正确计算有着重要意义。
书写化学式的记忆口诀:
正价前,负价后;金属左,
非金右,氧化物中氧在后。
①原子团的个数是1时,1省略不写,不需要加括号;如果原子团的个数是2或3时,把原子团加括号,在括号的右下角标上数字。
②+2价的铁称亚铁。
③绝不能根据化合价随意乱造事实上不存在的物质的化学式。
一般说来,有的单质是由原子构成的,由原子构成的单质,它们的化学式直接用元素符号直接去表示。
有的单质由分子构成,它们的化学式:先写出元素符号,在元素符号的右下角加上数字“2”。
学习化合价的方法:
对于化合价的概念,不需要理解多深,只要能记住会用,会根据化合物中化合价的代数和等于零的原则书写化学式即可。
为了能够熟练、快速、准确地书写化学式,要记住常见元素或原子团的化合价。计算元素的化合价首先要记住常见元素的化合价,其次要了解化合价遵守的法则,即在一切化合物里,正、负化合价的代数和一定为零,以不变应万变。
记忆化合价的口诀:
一价钾钠氢氯银,二价钙镁钡锌氧
三价铝四价硅,二三铁,二四碳
二四六硫都齐全,铜汞二价最常见
常见原子团的化合价:
负一硝酸氢氧根,负二硫酸碳酸根,正一价的是铵根。
原子团:在化学反应中并不是所有的时候都是作为一个整体参加反应;原子团不能单独存在,必须与其他的原子或原子团结合才能成为物质的化学式。
化合价只有在元素之间形成化合物时才能表现出来,当元素以单质的形式存在时,其化合价定为零。
疑难导析
化学式表示的意义可从宏观和微观两个方面进行论述:宏观上表示什么,微观上表示什么。
化学式表示的意义还可以从量的方面进行论述:如是否表示分子中的原子数,是否表示分子中各原子的个数比等。
化合价的规律要从以下几方面论述:
一是要说明在化合物里,氧、氢通常的化合价及氧原子的电子层结构,电子的得失及电子对的偏向趋势;金属元素通常的化合价及金属原子的电子层结构,电子的得失;非金属元素通常的化合价及原子的电子层结构,电子的得失及电子对的偏向趋势;非金属氧化物里,氧的化合价,另一种非金属元素的化合价。
二是在化合物里,正、负化合价的关系。
三是在单质中元素的化合价。
四是有些元素的化合价的可变性及其原因。
五是某些原子团的化合价及其计算方法。
问题导思
在计算质量分数时,一定把所求元素的原子个数找清楚,不要漏掉,如例题中每个硝酸铵分子中含有2个氮原子。因此计算氮的质量分数时一定要注意用氮的相对原子质量乘以2。
有时在进行此类题的计算时,通常先计算物质中某元素的质量。一定量的某物质中所含某元素的质量与该物质的质量、该元素在化合物中的质量分数之间的关系。
典题导考
绿色通道
明确化学符号周围各数字的含义:化学符号前的数字表示粒子的个数;右下角表示每个粒子中所含有该原子的数目;右上角表示离子所带的电荷数;正上方表示这种元素在化合物中表现出来的化合价。
典题变式
写出下列数字“2”的意义:
(1)2H:___________________________________________。
(2)H2:___________________________________________。
(3)2H2O:___________________________________________。
答案:(1)两个氢原子;(2)每个氢分子含两个氢原子;(3)前面的“2”表示两个水分子,右下角的“2”表示每个水分子含有两个氢原子。
绿色通道
常规解法是根据元素的质量分数=化合物中某元素的相对原子质量×该元素的原子个数/化合物的相对分子质量×100%。
典题变式
在铁的三种氧化物FeO、Fe2O3、Fe3O4中,铁元素的质量分数由大到小的排列顺序为( )
A.FeO>Fe2O3>Fe3O4 B.Fe2O3>Fe3O4>FeO
C.Fe3O4>Fe2O3>FeO D.FeO>Fe3O4>Fe2O3
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com