

题目列表(包括答案和解析)
26.(8分)在一定体积的密闭容器中,进行如下化学反应:

其化学平衡常数K和温度t的关系如下表:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________________。
(2)该反应为_________反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是__________(多选扣分)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: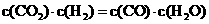 ,试判断此时的温度为____________℃。
,试判断此时的温度为____________℃。
四附加题(共10分)
25.(8分)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,反应达平衡时有3molSO2发生了反应。试填写下列空格:
(1)SO2的转化率为___________________;
(2)平衡时体系中SO2的百分含量(体积分数)为____________;
(3)平衡时c(O2)=______________mol/L;
(4)平衡时容器内气体压强与反应前的压强之比为___________。(最简整数比)
24.(8分)在一定条件下, 的反应达到平衡。
的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是_______________
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向________移动。
(填“正向”、“逆向”或“无法判断”)
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是______________态。(填“气”、“液”或“固”)
(4)加热后C的质量分数减少,则正反应是__________热反应。(填“吸”或“放”)。
23.(3)红磷(P)和白磷(P4)均为磷的同诉异形体。已知:
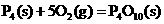
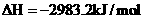
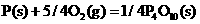

写出白磷转化为红磷的热化学方程式___________________________________,
由此可知,红磷比白磷______________。(填“稳定”或“不稳定”)
22.(2分)在25℃、101kPa下,已知拆开1
mol H-H键,1molN-H键,1molN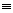 N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________________________________________________。
N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________________________________________________。
21.(6分) 已知下列两个热化学方程式:
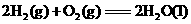
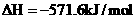
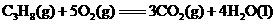
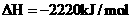
(1) 的燃烧热为________________,
的燃烧热为________________,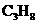 的燃烧热为_________________。
的燃烧热为_________________。
(2)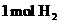 和
和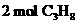 组成的混合气体完全燃烧释放的热量为_____________。
组成的混合气体完全燃烧释放的热量为_____________。
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3847kJ,则在混合气体中H2和C3H8的体积比是____________________。
20. (10分)一定温度下,在2L容器中某一反应的A、B物质的量随时间变化的曲线如右图所示,由图中数据分析得:
(10分)一定温度下,在2L容器中某一反应的A、B物质的量随时间变化的曲线如右图所示,由图中数据分析得:
 (1)该反应的化学方程式为_____________________。
(1)该反应的化学方程式为_____________________。
 (2)反应开始至4min时,A的平均反应速率为____________。
(2)反应开始至4min时,A的平均反应速率为____________。
 (3)正逆反应速率的大小关系,4min时,v正________v逆;From:k%s^5*u8min时,v正________v逆。(填“
(3)正逆反应速率的大小关系,4min时,v正________v逆;From:k%s^5*u8min时,v正________v逆。(填“ ”,“
”,“ ”或“=”)。
”或“=”)。
(4)若正反应是放热反应,则升高温度时B的百分含量________。(填“增大”、“减小”或“不变”)。
19. (9分)反应
(9分)反应 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。

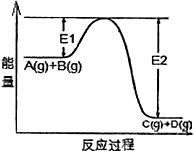 (1)该反应是__________________反应(填“吸热”或“放热”);
(1)该反应是__________________反应(填“吸热”或“放热”);
 (2)当反应达到平衡时,升高温度,A的转化率__________,(填“增大”“减小”“不变”),原因是__________________
___________________________________________________。
(2)当反应达到平衡时,升高温度,A的转化率__________,(填“增大”“减小”“不变”),原因是__________________
___________________________________________________。
 (3)反应体系中的加入催化剂对反应热是否有影响? __________,原因是_________________________________。
(3)反应体系中的加入催化剂对反应热是否有影响? __________,原因是_________________________________。
 (4)在反应体系中加入催化剂,反应速率增大,E1和E2的变
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变
 化是:
化是: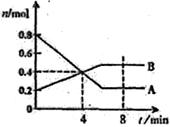 E1_________,E2________(填“增大”、“减小”或“不变”)。
E1_________,E2________(填“增大”、“减小”或“不变”)。
18. X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应: ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
 A.33%
B.40%
C.50%
D.65%
A.33%
B.40%
C.50%
D.65%


 第II卷(共46分)
第II卷(共46分)
17. 判断反应过程自发性的目的是
判断反应过程自发性的目的是
 A.判断反应的方向
B.确定反应是否一定发生
A.判断反应的方向
B.确定反应是否一定发生
 C.判断反应过程发生的速率 D.判断反应过程的热效率
C.判断反应过程发生的速率 D.判断反应过程的热效率
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com