
题目列表(包括答案和解析)
20.(16分)某有机物X(C12H13O6Br)遇到FeCl3溶液显紫色,其部分结构简式如下:
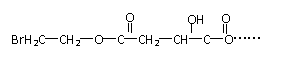
(注:图中的虚线指未给出的部分)
已知,X在足量的氢氧化钠水溶液中加热,可以得到A、B、C三种有机物。且知:
①B、C的核磁共振氢谱吸收峰分别是1个峰和2个峰。
②室温下A经盐酸酸化可以得到苹果酸E,E的结构简式为
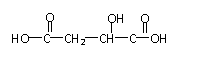
试根据以上信息回答:
(1)C中所含官能团的名称是___________________________。
(2)B的结构简式为___________________________________。
(3)E不能发生的反应类型是___________________________。(填序号)
①加成反应 ②消去反应 ③氧化反应 ④酯化反应
(4)在A、B、C三种有机物中,其中含有手性碳原子的物质的结构简式为____________。
(5)E的一种同分异构体F有如下特点:lmol F可以和3mol金属钠发生反应,放出33.6L H2(标准状况下),lmolF可以和足量NaHCO3溶液反应,生成lmolCO2,lmolF还可以 发生银镜反应,生成2molAg。试写出符合上述条件的F可能有的结构简式(两个羟基不能同时连在同一碳原子上):___________________________________________________。
(6)请用合成反应流程图表示出以1,3-丁二烯为主要有机原料合成苹果酸E的最合理的合成方案(注明反应条件)。
提示:①有机物必须写结构简式,无机试剂自选;
② 合成反应流程图表示方法示例如下:

19. (13分)相对分子质量为94.5的饱和有机物A(含C、H、O、Cl四种元素),在一定条件下可以发生如下图所示的转化(其他产物和水已略去):
(13分)相对分子质量为94.5的饱和有机物A(含C、H、O、Cl四种元素),在一定条件下可以发生如下图所示的转化(其他产物和水已略去):
|
回答下列问题:
(1)写出下列物质的结构简式:
F___________________________,H___________________________。
(2)写出下列反应的化学方程式:
A→B___________________________;D→G____________________;
E与新制银氨溶液反应______________________________________。
18.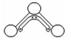 (8分)1949年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如下图所示:呈V型,键角116.5° 。三个O原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;此外中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键(虚线内部分)- 三个O原子均等地享有这4个电子。请回答:
(8分)1949年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如下图所示:呈V型,键角116.5° 。三个O原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;此外中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键(虚线内部分)- 三个O原子均等地享有这4个电子。请回答:
(1)从电子云重叠方式看分子中存在的非极性共价键是_________键,
特殊的化学键是_________键。(填“σ”或“π”)
(2)下列物质的分子与O3分子的结构最相似的是_________。
A.H2S B.SO2 C.CS2 D.BeCl2
(3)原子最外层电子中没有跟其他原子共用的电子对叫孤对电子,那么O3分子有______对孤对电子。
(4)下列有关说法中不正确的是_________。
A.等质量的O2和O3分子中所含氧原子数之比为2:3
B.O2和O3互为同素异形体,且O3的氧化性比O2强,O3可用于杀菌、消毒
C.大气中O3过多会对人体造成危害
D.通常由O3分解成O2的过程中需要吸收能量
E.向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解
17.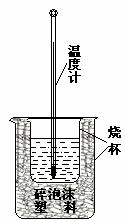 (7分)
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在
(7分)
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在
如图所示的装置中进行中和反应。通过测定反应过程中所
放出的热量可计算中和热。回答下列问题:
①该图中有两处未画出,它们是 、 ;
②在操作正确的前提下提高中和热测定的准确性的关键
是 ;
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中
所测出的“中和热”将 (填“偏大”、“偏小”、“不变”);
原因是
。
16. (10分)下图甲是实验室旧法制取溴苯的装置,乙是新设计的改进装置。
(10分)下图甲是实验室旧法制取溴苯的装置,乙是新设计的改进装置。
已知:制备溴苯的反应是一个放热反应,溴苯在通常情况下与NaOH难反应。试通过分析回答下列问题:
①实验仪器安装好后在加药品前应进行的操作是_______________
②乙中冷凝水的进口应为_______________(填“a”或“b”)
③乙中反应结束后,应先进行的操作是_______________
④乙装置与甲装置相比较有哪些优点(答出主要的两点)_______________
15.(3分) 现有三种白色粉末A、B、C均可作为抗酸药物的有效成分, A、B难溶于水,也不溶于NaOH溶液,C易溶于水,和胃酸反应,A和C都能产生使澄清石灰水变浑浊的气体,但B不能产生气体.根据以上现象完成下列填空:
(1) C是________________(名称或化学式)
(2) 写出A、B分别和胃酸反应的化学方程式:
____________________________________________________________________
____________________________________________________________________
14.常温时,将两种溶液等体积混合,其中溶液pH一定或可能等于7的情况共有( )
①pH=2盐酸和pH=12 NaOH溶液 ②pH=2醋酸和pH=12 NaOH溶液
③pH=2盐酸和pH=12氨水 ④pH=2某酸和pH=12 NaOH溶液
⑤pH=2盐酸和pH=12某碱溶液 ⑥pH=2硫酸和pH=12 NaOH溶液
⑦pH=2盐酸和pH=12 Ba(OH)2溶液 ⑧pH=2硫酸和pH=12 Ba(OH)2溶液
A.5种 B.6种
C.7种 D.8种
第Ⅱ卷 (非选择题 共72分)
13.一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 ( )
3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 ( )
A.2mol C B.2mol A 1mol B和1mol He
C. 1mol B和1mol C D.2mol A 3mol B和3mol C
12.已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是 ( )
A.CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
B.在相同条件下,两溶液的pH大小为: CH3COONa< NaF
C.NaF溶液中:c(H+)+c(HF)= c(OH-)
D.两溶液相比较,NaF溶液中的离子总数较多
11.食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是 ( )
A.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
B.Cl-CH2COOH既能发生中和反应、取代反应又能发生消去反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com