
题目列表(包括答案和解析)
7、下列化学用语的书写,正确的是
A、氮气的电子式: B、硫原子的结构示意图:
B、硫原子的结构示意图:
C、溴化钠的电子式: 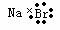 D、水分子的结构式:
D、水分子的结构式:
6、下列各对原子序数的原子能以共价键结合成化合物的是
A、9和11 B、15和17 C、11和8 D、12和17
5、下列物质,既含离子键又含共价键的是
A、Na2S B、NH3 C、MgCl2 D、NaOH
4、在元素周期表中金属元素与非金属元素的分界线附近的一些元素能用于制
A、合金 B、催化剂 C、半导体 D、农药
3、关于199F-微粒叙述正确的是
A、质量数为19,电子数为9 B、质子数为9,中子数为10
C、质子数为9,电子数为9 D、中子数为10,电子数为8
2、硅的原子序数为14,那么硅元素在周期表中的位置是
A、第3周期,ⅣA族 B、第3周期,ⅥA族
C、第2周期,ⅣA族 D、第2周期,ⅥA族
1、对元素周期表和元素周期律的发现有突出贡献的科学家是
A、拉瓦锡 B、门捷列夫 C、阿伏加德罗 D、居里夫人
16、(1)ΔH < 0(填<、=、>)
(2)_不影响__,原因是_ 催化剂不改变平衡的移动 :
 (3)E1 减小__,E2___减小 __(填“增大”“、”“不变”)。
(3)E1 减小__,E2___减小 __(填“增大”“、”“不变”)。
(4)_____ C (填字母)。理由是_该反应达到平衡时,平衡常数K=
增大容器体积时,c(CH3OH)和c(CO)等比例减小,由于H2浓度不变,此时的值仍然等于K,所以平衡不移动_。
(5)结论一:在一定条件下,反应温度越高,碳转化率 _ 越高__ __;
结论二:_原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高碳转化率又降低且有甲烷生成____ 。
15、(1)
 (2)
X + 2Y
(2)
X + 2Y  2Z
;
2Z
;
(3) 1/6 mol·L-1 ·min-1 ;
(4) 55 ﹪ __。
14、
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 ③ 探究温度对该反应速率的影响; (Ⅲ)实验①和 ④ 探究规格(粗、细)对大理石该反应速率的影响;) |
|
② |
298 |
粗颗粒 |
1.00 |
|
|
③ |
308 |
粗颗粒 |
2.00 |
|
|
④ |
298 |
细颗粒 |
2.00 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com