
题目列表(包括答案和解析)
24、一定温度下的密刚容器中存在如下反应:2SO (g)+
(g)+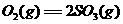 ,已知
,已知
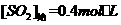 ,测定该反应在该温度下的平衡常数K≈19
,测定该反应在该温度下的平衡常数K≈19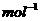 ·L,试判断:
·L,试判断:
(1)当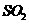 转化率为50%时,该反应是否达到平衡状态?若未达到,向哪个方向进行?
转化率为50%时,该反应是否达到平衡状态?若未达到,向哪个方向进行?
(2)在平衡状态时,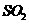 的转化率应为多少?
的转化率应为多少?

22、(5分)实验室中配制碘水,往往是将I2溶于Kl溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反
应:
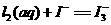 上述平衡体系中,I
上述平衡体系中,I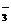 的物质的量浓度c(I
的物质的量浓度c(I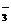 )与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。
)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。
(1)通过分析上图,该反应的正反应为 反应(填“吸热”或“放热”)。
(2)在T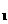 、D状态时,V(正)
、D状态时,V(正) 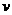 (逆)(填“>”、“<”或“=”)。
(逆)(填“>”、“<”或“=”)。
(3)写出该平衡常数的表达式K= 。若升高温度,K值将 (填“增大”、
“减小”或“不变”,下同);若将溶液中加入少量的溴水,K值将 。
21、(12分)清用下图所示装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
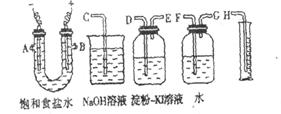
(1)所选仪器连接时,各接口的连接顺序是(填各接口的字母):A接 ,
B接 。
(2)实验时,装置中的石墨电极接电源的 极,所发生的电极反应式为
;铁电极接电源的 极,所发生的电极反应方程式为
 ;此电解总反应方程式为 。
;此电解总反应方程式为 。
20、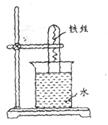 (9分)如右图所示,大试管里放入一段光亮无锈的弯成螺旋状的铁丝,试管倒插入液面下,放置约一周后,观察到铁丝发生的变化是
(9分)如右图所示,大试管里放入一段光亮无锈的弯成螺旋状的铁丝,试管倒插入液面下,放置约一周后,观察到铁丝发生的变化是
(1)若试管内液面上升,则原溶液呈 性,发
生 腐蚀,则最终上升高度约为 ,
正极电极反应式 。
(2)若试管内液而下降,则原溶液呈一性,发生 腐蚀,电极反应式为:负极
;正极 。
19、 某实验小组用0.50 mol·L
某实验小组用0.50 mol·L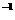 NaOH溶液和0.50
mol·L
NaOH溶液和0.50
mol·L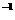 硫酸进行中和热的测定。
硫酸进行中和热的测定。
 I配制0.50 mol·L
I配制0.50 mol·L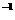 NaOH溶液
NaOH溶液
 (1)若实验中大约要使用245 mL
NaOH溶液,至少需要称量NaOH固体
g。
(1)若实验中大约要使用245 mL
NaOH溶液,至少需要称量NaOH固体
g。
 (2)从下图中选择称量NaOH固体所需要的仪器:
(填字母)。
(2)从下图中选择称量NaOH固体所需要的仪器:
(填字母)。
|
名称 |
托盘天平 (带砝码) (带砝码) |
小烧杯 |
坩埚钳 |
玻璃棒 |
药匙 |
量筒 |
|
仪器 |
 |
 |
 |
 |
 |
 |
|
序号 |
a |
b |
c |
d |
e |
F |


 II、测定稀硫酸和氧化钠溶液反应中和热(实验装置如右图所示)。
II、测定稀硫酸和氧化钠溶液反应中和热(实验装置如右图所示)。
 (1)写出该反应的热化学方程式:
(1)写出该反应的热化学方程式:
 (中和热为57.3kJ·mol
(中和热为57.3kJ·mol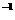 )。
)。
 (2)每次分别取50mL NaOH溶液和30mL硫酸进行实验,实验数据如下表。
(2)每次分别取50mL NaOH溶液和30mL硫酸进行实验,实验数据如下表。
 温度 温度 实验 实验 次数 次数 |
起始温度 |
终止温度 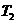 /°C /°C |
温度差 ( (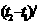 °C) °C) |
||
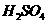 |
 |
平均值 |
|||
|
1 |
26.2 |
26.0 |
26.1 |
30.1 |
4.0 |
|
2 |
27.0 |
27.4 |
27.2 |
33.3 |
6.1 |
|
3 |
25.9 |
25.9 |
25.9 |
29.8 |
3.9 |
|
4 |
26.4 |
26.2 |
26.3 |
30.4 |
4.1 |
 ①若近似认为0.5mol·L
①若近似认为0.5mol·L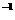 NaOH溶液和0.5mol·L
NaOH溶液和0.5mol·L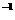 硫酸的密度都是1g·cm
硫酸的密度都是1g·cm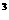 ,中和后生
,中和后生
 成溶液的比热容为4.18kJ·K
成溶液的比热容为4.18kJ·K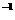 ·kg
·kg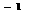 ,则中和热
,则中和热
 △H=
.
△H=
.
②上述实验数值结果与57.3kJ·mol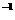 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是
(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定Na0H溶液起始温度后直接测定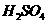 溶液的温度
溶液的温度
18、 金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备
金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备
 高纯度的镍,下列叙述正确的是
高纯度的镍,下列叙述正确的是
 (已知,氧化性
(已知,氧化性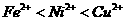 )
)
 A、阳极发生还原反应,其电极反应式:
A、阳极发生还原反应,其电极反应式: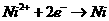
 B、电解过程中,阳极质量的减少与阴极质量的增加相等
B、电解过程中,阳极质量的减少与阴极质量的增加相等
 C、电解后,电解槽底部的阳极泥中含有Cu和Pt
C、电解后,电解槽底部的阳极泥中含有Cu和Pt
 D、电解后,溶液中存在的金属阳离子只有Fe
D、电解后,溶液中存在的金属阳离子只有Fe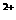 和Zn
和Zn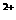

 第II卷(非选择题
共46分)
第II卷(非选择题
共46分)
11. 2L(标准状况)的气体,则原溶液中的NaCl的物质的量浓度不可能为
2L(标准状况)的气体,则原溶液中的NaCl的物质的量浓度不可能为
 A.
A. B.
B.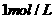
 C.
C. D.
D.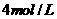
17、 用惰性电极电解NaCl和CuSO
用惰性电极电解NaCl和CuSO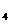 的混合溶液250mL,经过一段时间后,两极分别得到
的混合溶液250mL,经过一段时间后,两极分别得到
16. 下列叙述正确的是
下列叙述正确的是
 ①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
 ②镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
②镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
 ③电镀时,应把镀件置于电解槽的阴极
③电镀时,应把镀件置于电解槽的阴极
 ④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解
④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解
 ⑤钢铁表面常易锈蚀生成
⑤钢铁表面常易锈蚀生成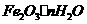
 A、①②③④⑤ B、①③④⑤
A、①②③④⑤ B、①③④⑤
 C、①③⑤ D、②④
C、①③⑤ D、②④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com