
题目列表(包括答案和解析)
17. 某温度时,AgCl (s)
某温度时,AgCl (s)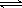 Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
( )
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
( )
A.加入AgNO3可以使溶液由c点变到d点
B.加入固体NaCl则AgCl的溶解度减小,Ksp也减小
C.c点对应的Ksp小于a点对应的Ksp
D. d点有AgCl沉淀生成
16.相同温度下,将足量的AgCl分别放入下列溶液中,AgCl的溶解程度的大小顺序为( )
①20 mL0.1mol·L-1 (NH4)2CO3溶液 ②40mL0.02mol·L-1 BaCl2溶液
③40mL0.03mol·L-1盐酸 ④10mL蒸馏水 ⑤50mL0.05mol·L-1 AgNO3溶液
A.①=②=③=④=⑤ B.①>④>③>②>⑤
C.⑤>④>①>②>③ D.④>③>⑤>①>②
15.已知常温、常压下,饱和CO2溶液的pH为3.9,则可推断用已知浓度的盐酸滴定未知浓度的NaHCO3溶液时,应选用的指示剂及滴定终点的颜色变化是 ( )
A.石蕊、由蓝变红 B.酚酞、红色褪去
C.甲基橙,由橙变黄 D.甲基橙、由黄变橙
14.有甲、乙两醋酸稀溶液,测得甲的pH=a,乙的pH=a+1。下列推断中正确的是( )
A.物质的量浓度c(甲)=10c(乙)
B.甲中由水电离产生的H+的物质的量浓度是乙的0. 01倍
C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)>10V(甲)
D.甲中的c(OH-)为乙中c(OH-)的10倍
13.氯化铜的稀溶液是淡蓝色的,可是加入浓盐酸后,溶液变成黄绿色了,这种颜色变化是由下列可逆反应造成的:Cu(H2O)42+(溶液)+4Cl-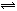 CuCl42-(溶液)+4H2O其中Cu(H2O)42+为淡蓝色,CuCl42-为黄绿色。下列哪种方法能使溶液变成淡蓝色:
(
)
①加蒸馏水, ②加AgNO3溶液,
③加入NaCl溶液, ④加入NaOH溶液。
CuCl42-(溶液)+4H2O其中Cu(H2O)42+为淡蓝色,CuCl42-为黄绿色。下列哪种方法能使溶液变成淡蓝色:
(
)
①加蒸馏水, ②加AgNO3溶液,
③加入NaCl溶液, ④加入NaOH溶液。
A.只有① B.只有② C.①和② D.③和④
12.向0.1 mol·L-1的CH3COOH溶液中加入CH3COONa晶体或加水稀释时,会引起 ( )
A.溶液的pH都增加 B.CH3COOH电离程度增大
C.溶液导电能力都减弱 D.溶液中c(OH-) 都减小
11. 下列离子方程式书写正确的是: ( )
A.硫酸氢钠溶液与氢氧化钡溶液混合呈中性:H++SO42-+Ba2++OH-=BaSO4↓+ H2O
B.硫酸氢钠溶液与氢氧化钡溶液反应后,硫酸根离子完全沉淀:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
C.明矾溶液与过量氢氧化钡溶液反应:
Al3+ + SO42- + Ba2+ + 4OH- =BaSO4↓+ AlO2- +2H2O
D.明矾与氢氧化钡溶液混合接近呈中性:
2Al3++3SO42-+3Ba2++6OH- = 3BaSO4↓+2Al(OH)3↓
10.常温下,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH-)=10-24,则下列各组离子在该溶液中一定可以大量共存的是 ( )
A.K+、Na+、A1O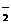 、Cl-
B.Na+、C1-、SO
、Cl-
B.Na+、C1-、SO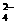 、HCO
、HCO
C.NH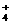 、Na+、NO
、Na+、NO 、SO
、SO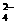 D.Ba2+、Na+、C1-、NO
D.Ba2+、Na+、C1-、NO
9. 已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO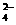 .某温度下,向pH=6的蒸馏水
.某温度下,向pH=6的蒸馏水
中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中不正确的是 ( )
A.该盐溶液不存在水解
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
8.已知某溶液中存OHˉ、H+、NH4+和C1ˉ四种离子,其浓度大小有如下关系 ( ) ①c(C1ˉ)>c(NH4+)>c(H+)>c(OHˉ)
②c(C1ˉ)>c(H+)>c(NH4+)>c(OHˉ)
③c(C1ˉ)=c(NH4+)且c(OHˉ)=c(H+)
④c(OHˉ)>c(H+)>c(C1ˉ)>c(NH4+)
⑤c(H+)>c(OHˉ)>c(C1ˉ)>c(NH4+)其中可能的是
A.①②④ B.②③⑤ C.①②③ D.③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com