
题目列表(包括答案和解析)
6. 已知某可逆反应mA(g)+ nB(g) pC(g);⊿H?。在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
已知某可逆反应mA(g)+ nB(g) pC(g);⊿H?。在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
A、T1<T2、P1>P2、m+n>P1,⊿H <0;
B、T1>T2、P1<P2、m+n>P1、⊿H >0;
C、T1<T2、P1>P2、m+n<P1,⊿H <0;
D、T1>T2、P1<P2、m+n<P1、⊿H >0;
5. 已知某温度下的热化学方程式:2SO2(气)+O2(气) 2SO3;△H= -197KJ/mol,在同温同压下,向密闭容器中通入2molSO2和1molO2,达平衡时放出热量Q1KJ;向另一相同的密闭容器中通入1.5molSO2,0.75molO2和0.5molSO3,达平衡时放出热量Q2KJ。下列关系正确的是
A.Q1=Q2=197 B.Q1=Q2<197 C.Q1<Q2<197 D.Q2<Q1<197
4. 下列推论正确的是
A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2
B.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则:由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ/mol,则:含20gNaOH的溶液与稀盐酸完全反应,放出的热量为28.7kJ
D. CaCO3(s)=CaO(s)+CO2(g) △H>0,△S>0,则:该反应任何温度下都能自发进行
3. 下列物质的水溶液能导电,但属于非电解质的是( )
A.CH3COOH B.SO2 C.(NH4)2CO3 D. Cl2
2. 下列说法正确的是( )
A.熵增大的反应一定可自发进行 B.熵减小的反应一定可自发进行
C.ΔH<0的反应可能自发进行 D.ΔH>0的反应不可能自发进行
1.已知在1×105 Pa,298 K条件下,2mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.H2O(g) = H2(g) +  O2 (g) △H = +242 kJ/mol
O2 (g) △H = +242 kJ/mol
B.2H2(g) + O2 (g) = 2H2O (l) △H = -484 kJ/mol
C.H2 (g) +  O2 (g) = H2O (l) △H = -242 kJ/mol
O2 (g) = H2O (l) △H = -242 kJ/mol
D.2H2 (g) + O2 (g) = 2H2O (g) △H = +484 kJ/mol
※内容安排:第一章占15%左右,第二章占25%左右,
第三章占30%左右,第四章占30%左右。
※试题信息采取方法:每节2个选择题(个别节1个),主要用教材上的习题改编;非选择题主要取材教材内容(包括实验内容)。
※难易题比例,均采用2分一个得分点;容易题约30分,中等难度的题约55分,难题约15分。
※复习建议:读教材和做教材中的习题。
32.(8分)某铅蓄电池的正、负极标记被磨损。试用下图装置设计实验,识别出此铅蓄电池的正负极。

(1)若A接E,B接F,而B电极出现 ,反应式为 ,则说明F为正极;
(2)某学生试图用上述装置,根据电极上析出的物质的质量来测定阿伏加德常数的值。通电时间t s,测定通过电路的电流强度为I。精确测得A电极析出铜的质量的操作包括以下几步:
①低温烘干电极后称量
②用蒸馏水清洗电解后的电极
③称量电解前的电极质量
④再次低温烘干后称量
正确的操作顺序是 ;
(3)若经过上述操作测定生成铜的质量为mg,试列出计算阿伏加德罗常数的表达式(已知一个电子电量为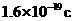 ):
): =
=

说 明
※试卷结构:模拟学业水平考试试卷。
31.(8分)设计实验证明弱酸的酸性:醋酸>碳酸>硼酸。提供的试剂有: 溶液、
溶液、 溶液、
溶液、 溶液、硼酸(
溶液、硼酸( )溶液、
)溶液、 溶液、
溶液、 溶液。
溶液。
(1)证明酸性醋酸>碳酸的操作方法是(简述): ,化学方程式是 。
(2)证明酸性碳酸>硼酸的操作方法是(简述): ,得出“酸性碳酸>硼酸”的结论的现象或理由是(简述) 。
30.(8分)下图是一些常见的物质间的转化关系图。C是紫红色金属单质,G是蓝色沉淀,X是葡萄糖溶液,H是砖红色沉淀,F是形成酸雨的无色有害气体,所有反应物、生成物中的水均未标出;反应②的条件是使用浓B溶液和加热。

(1)A是 ,E是 ;
(2)电解A溶液时阴极的反应式 ;
(3)电解A溶液的总反应化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com