
题目列表(包括答案和解析)
23.(6分)请完成并配平反应
KMnO4+ H2S+ H2SO4= K2SO4+ MnSO4+ S↓+
该反应中电子转移总数是 ,当反应中有80 g硫析出时,有 mol还原剂被氧化。
22.(4分)下面是某学生用已知浓度的盐酸溶液测定未知浓度的NaOH溶液的部分操作,其中错误的是
A. 取一锥形瓶,用待测NaOH溶液润洗两次后装入25 mL待测NaOH溶液
B. 加入几滴石蕊试液作指示剂
C. 取一支酸式滴定管,洗涤干净后直接往其中注入标准盐酸溶液
D. 滴定时,两眼注视滴定管内盐酸溶液液面下降,直至滴定终点
21.(8分)现有浓度均为0.1 mol·L-1的四种电解质溶液:
①NaHCO3 ②NaAlO2 ③CH3COONa ④NaOH
|
(2)将四种溶液稀释相同倍数时,其pH变化最大的是 ▲ (填编号)。
(3)在上述四种溶液中,分别加入FeCl3溶液,能产生的共同现象是 ▲ ,能产生气体的 ▲ (填编号)。
20.下列方程式属于水解反应的是 ( )
A. H2O+H2O 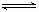 H3O++H+
H3O++H+
B. 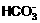 +H2O
+H2O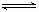 H3O++
H3O++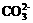
C. 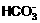 +OH-=H2O+
+OH-=H2O+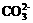
D. 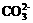 +H2O
+H2O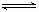
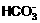 +OH-
+OH-
19.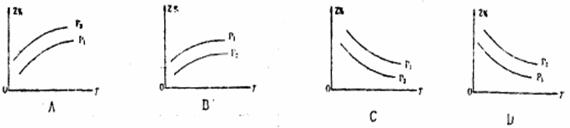 如图所示,反应X(g)+3Y(g)
如图所示,反应X(g)+3Y(g)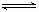 2Z(g)+Q,在不同温度、不同压强( P1<P2)下,达到平衡时,混合气体中Z的体积分数Z%随温度变化的曲线应为
( )
2Z(g)+Q,在不同温度、不同压强( P1<P2)下,达到平衡时,混合气体中Z的体积分数Z%随温度变化的曲线应为
( )
18.某无色透明溶液能与Al反应析出H2,则此溶液中可能大量存在的是 ( )
A. OH-、Ba2+、Cl-、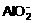 B. H+、Mg2+、
B. H+、Mg2+、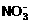 、Na+
、Na+
C. H+、Cu2+、 、K+
D. H+、Cl-、
、K+
D. H+、Cl-、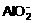 、Mg2+
、Mg2+
17.根据下列化学方程式
① 2 十16H+十10Cl-=2Mn2+十8H2O十5Cl2
十16H+十10Cl-=2Mn2+十8H2O十5Cl2
② 2Fe2++Cl2=2Fe3++2Cl-
③ 2Fe3++Cu=2Fe2++Cu2+
|
可推断 、Fe2+、Cu2+、Fe3+、Cl2的氧化性由强到弱的顺序为
( )
、Fe2+、Cu2+、Fe3+、Cl2的氧化性由强到弱的顺序为
( )
A.  >Cl2>Fe3+>Cu2+>Fe2+
>Cl2>Fe3+>Cu2+>Fe2+
B. Fe3+> >Cl2>Cu2+>Fe2+
>Cl2>Cu2+>Fe2+
C. Cl2> >Fe3+>Cu2+>Fe2+
>Fe3+>Cu2+>Fe2+
D. Cu2+>Cl2> >Fe3+>Fe2+
>Fe3+>Fe2+
16.20℃时H2S饱和溶液1 L,其浓度为0.1 mol / L,其电离方程式为H2S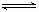 H++HS-,HS-
H++HS-,HS-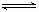 H++S2-,若要使溶液的pH值和C(S2-)减小,可采取的措施是
( )
H++S2-,若要使溶液的pH值和C(S2-)减小,可采取的措施是
( )
A. 通入适量的H2S气体 B. 加入少量的氢氧化钠固体
C. 加入适量的CuSO4固体 D. 加入适量水
15.在一定温度下的固定容积的密闭容器中,反应A2(g)+B2(g)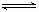 2AB(g),达到平衡的标志是
( )
2AB(g),达到平衡的标志是
( )
A. 单位时间内生成n mol A2,同时生成n mol AB
B. 容器内的总压强、密度和平均相对分子质量均不随时间变化
C. 容器内A2、B2、AB的物质的量之比1∶1∶2
D. 单位时间内生成2n mol的AB同时生成n mol的B2
14.1999年曾报导合成和分离了含高能量的正离子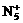 的化合物N5AsF6,下列叙述错误的
的化合物N5AsF6,下列叙述错误的
是 ( )
A. 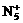 具有34个核外电子
具有34个核外电子
B. 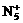 中氮-氮原子间以共用电子对结合
中氮-氮原子间以共用电子对结合
C. 化合物N5AsF6中As的价为+1价
D. 化合物N5AsF6中F的价为 -1价
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com