
题目列表(包括答案和解析)
1.所有不与水反应、难溶于水的气体都可用_______________法来收集。
化学是一门以______________为基础的科学。学习化学的一个重要途径是_______________,通过实验以及对实验现象的_______________、_______________和_______________等,可以发现和验证_______________,学习_______________并获得化学知识。在进行实验探究时,我们要关注以下几个方面的内容:
(1)关注_______________,如_______________、_______________、_______________、_______________、及_______________、_______________等等。
(2)关注_____________,如石蜡受热时是否_______________,燃烧时是否_______________、_______________并有_______________和_______________生成等等。
(3)关注_______________,即不是孤立地关注物质的某一种性质或变化,而是对物质在_______________、_______________和_______________的现象进行细致的观察和描述,并进行_______________,以得出可靠的结论。
答案:实验 实验 观察 记录 分析 化学原理 科学探究的方法
(1)物质的性质 颜色 状态 气味 硬度 密度 熔点 沸点
(2)物质的变化 熔化 发光 放热 二氧化碳气体 水蒸气
(3)物质的变化过程及其现象 变化前 变化中 变化后 比较和分析
2.用灼烧或加入熟石灰研磨的方法
|
|
氮肥 |
钾肥 |
||
|
硫酸铵 |
氯化铵 |
硫酸钾 |
氯化钾 |
|
|
灼烧 |
可燃烧,熔化或冒气泡 |
不燃烧,跳动或有爆裂声 |
||
|
加熟石灰研磨 |
放出刺激性气味的气体 |
无刺激性气味气体生成 |
||
结论:初步区分氮肥、磷肥、钾肥的方法
(1)看外观:氮肥、钾肥都是白色晶体,磷肥是灰白色粉末。
(2)加水:氮肥、钾肥都易溶于水;磷肥大多不易溶于水或部分溶于水。
(3)燃烧:氮肥可燃烧,熔化或冒气泡;钾肥不燃烧,灼烧时跳动或有爆裂声。
(4)加熟石灰研磨:含有铵根离子的氮肥能放出具有刺激性气味的氨气。
[示例] 化学肥料要合理使用,下列不宜与熟石灰混合使用的是( )
A.NH4NO3 B.KNO3 C.Ca3(PO4)2 D.K2SO4
解析:铵态氮肥与熟石灰混合会产生有刺激性气味的氨气,使化肥失效;A项含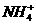 ,为铵态氮肥。
,为铵态氮肥。
答案:A
状元笔记
铵根离子(铵盐)的检验方法:加入碱溶液,有刺激性气味的气体放出,用湿润的红色石蕊试纸检验,变蓝色。(可简记为“铵盐遇碱生气”)据此可知,铵态氮肥不能与碱性物质混用,否则放出氨气,降低肥效。
活动与探究:初步区分氮肥、磷肥、钾肥的方法
1.比较外观和溶解性
|
|
氮肥 |
磷肥 |
钾肥 |
|||
|
碳酸氢铵 |
氯化铵 |
磷矿粉 |
过磷酸钙 |
氯化钾 |
硫酸钾 |
|
|
外观 |
白色晶体 |
白色晶体 |
灰白色粉末 |
灰白色粉末 |
白色晶体 |
白色晶体 |
|
气味 |
强烈气味 |
无味 |
无味 |
无味 |
无味 |
无味 |
|
溶解性 |
易溶 |
易溶 |
难溶 |
能溶 |
易溶 |
易溶 |
2.使用化肥和农药要注意的问题
化肥和农药是作物生长不可缺少的,但是不合理使用会带来一些环境问题。因为化肥和农药中都含有一些重金属和有毒有机物,过量使用不但不会增产,还会带来环境污染。近几年出现的“水华”和“赤潮”等水污染现象以及食品污染事件也与化肥农药的过量使用有关。因此要合理使用化肥、农药,既保证作物丰收,又尽量减少对环境的污染。
农作物生长需求量最大的营养元素是氮、磷、钾三种元素,因此氮肥、磷肥、钾肥是最重要的三种化肥。另外,复合肥是指含有两种或两种以上营养元素的化肥。
1.各种化肥的种类和作用


[示例](2008福州)碳铵(NH4HCO3)能使作物枝繁叶茂。碳铵属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
解析:根据碳铵的化学式可以看出,碳铵中含有的营养元素只有氮元素,故属于氮肥。
答案:C
状元笔记
各种化肥对作物的生长所起的作用不同,氮肥主要促使茎叶生长;磷肥主要使果实饱满和根系发达;钾肥主要使茎秆健壮,增强抗病、抗倒伏能力。
4.已知一个碳原子的质量为1.993×10-26kg,铝的相对原子质量为27,则一个铝原子的质量为( )
A.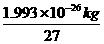 ×12
B.
×12
B.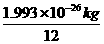 ×27
×27
C.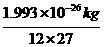 D.27 g
D.27 g
答案:B 解析:根据相对原子质量的概念,其他原子跟碳原子质量的1/12作比较所得的值就是这种原子的相对原子质量。可设铝原子的质量为x,列计算式:x÷(碳原子的质量×1/12)=27,再转化为计算式就可得到正确答案。
探究:相对原子质量的引入,简化了我们记忆与计算的烦琐程度,在学习中要注意以下几点:
(1)相对原子质量只是一个比值,不是原子的实际质量,其单位不是克、千克等,国际上统一规定为一,符号为1,常省略不写;(2)原子的实际质量越大,则它的相对原子质量越大;原子的质量主要集中在原子核上,核外电子的质量非常小,常忽略不计,故有:相对原子质量≈质子数+中子数。
[例题2]科学家计划用质子数为20的钙离子,轰击核电荷数为98的锎元素靶,使两元素的原子核合并在一起,合成质子数为118的新元素。对此,下列理解正确的是( )
A.新元素的原子核外电子数为98 B.新元素的核电荷数为118
C.新元素的相对原子质量为118 D.变化过程中元素种类没有发生改变
解析:在原子中,核电荷数=质子数=核外电子数,故新元素的核电荷数和核外电子数均为118,A错误,B正确;由相对原子质量≈质子数+中子数,新元素原子的质子数为118,相对原子质量不可能为118,C错误;变化过程中质子数发生变化,元素种类亦发生变化,D错误。
答案:B
黑色陷阱:本题考查了构成原子的各粒子间以及它们与相对原子质量的关系。很多同学在解题时易将它们弄混,如把质子数当成相对原子质量,要注意记清以下关系:核电荷数=质子数=核外电子数,相对原子质量≈质子数+中子数。
针对训练:
3.最近科学家制造出原子序数为112号的新元素,其相对原子质量为277,下列有关112号元素的说法正确的是( )
A.该元素原子的中子数为112
B.该元素原子的质子数为165
C.该元素原子的核外电子数为112
D.该元素原子的核电荷数为277
答案:C 解析:在原子中,原子序数=质子数=核电荷数=核外电子数,由该原子的原子序数为112,可知B、D错误,C正确;相对原子质量=质子数+中子数,则该原子的中子数=相对原子质量-质子数=277-112=165,故A错误。
2.将正确的说法填在横线上______________________________________。
A.原子是构成物质的一种粒子
B.因为二氧化碳里含有氧分子,所以二氧化碳也具有氧气的化学性质
C.一切原子核都是由质子和中子构成的
D.原子的质量主要集中在原子核上
E.原子中质子和中子所带电荷量相等,电性相反,所以整个原子不显电性
答案:AD 解析:构成物质的粒子有多种,有些物质是由分子构成的,如氧气、水等,有些物质是由原子直接构成的,如铁、氩等,故A正确;二氧化碳属于纯净物,它是由同一种分子--二氧化碳分子构成的,每个二氧化碳分子又是由一个碳原子和两个氧原子构成的,其中并不含氧分子,也就不具有氧气的化学性质,故B错误;绝大多数原子核都是由质子和中子构成的,但是有一种最常见的氢原子核却只有一个质子,而没有中子,故C错误;原子是由原子核和核外电子构成的,原子核又是由质子和中子构成的,由于电子的质量很小,一个电子的质量约等于一个质子(或一个中子)质量的1/1 836,所以原子的质量主要集中在原子核上,故D正确;原子中中子不带电,故E错误。
探究:理解原子的构成(结构)是学好化学的基础之一。在化学变化中原子不能再破裂,它是化学变化中的最小粒子,但它不是不可再分割的实心球体,1897年英国科学家汤姆生发现电子,证明原子可再分。在学习中要牢记构成原子的粒子:核(原子核)、质(质子)、中(中子)、电(电子)。每个质子带1个单位的正电荷,每个电子带1个单位的负电荷,中子不带电,整个原子对外不显电性。同时还应注意以下几点:
(1)构成原子的粒子有三种:质子、中子、电子,但并不是所有的原子都是由这三种粒子构成的,如有一种氢原子不含中子;(2)现代原子能的利用、原子弹的爆炸等就是原子核裂变的结果,也证明原子核可以继续再分;(3)在原子中,核电荷数(即原子核所带的正电荷数)=质子数=核外电子数(原子呈中性)。
[例题1]为了揭开原子内部结构的奥秘, 1911年著名物理学家卢瑟福等人做了一个著名的“卢瑟福实验”:用一束带正电的质量比电子大得多的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,甚至有极少数的α粒子被反弹了回来。通过这一实验现象不能够获得的结论是( )
A.原子核质量较大 B.原子核体积很小
C.核外电子带有负电荷 D.原子核带有正电荷
解析:由于核外电子质量很小,可忽略不计,它对α粒子的运动不会造成影响,故在此实验中无法得出核外电子带负电荷的结论。
答案:C
绿色通道:本题是探究原子结构的著名实验。大多数α粒子能穿过金箔且不改变原来的前进方向,说明构成原子的各粒子间是有空隙的,也说明电子质量非常小,不会对α粒子的运动产生影响;小部分α粒子改变了原来的方向是由于距原子核较近,受到斥力,说明原子核带有正电荷;极少数的α粒子被反弹了回来,说明原子核体积很小,但质量较大。
针对训练:
1.中国探月计划第三期工程时间定在2011-2020年,目标是月面巡视勘察与采样返回。其中前期主要是研制和发射新型软着陆月球巡视车,对着陆区进行巡视勘察。探月的重要目的之一是勘察、获取月球上极为丰富的核聚变燃料--“He3”,解决地球能源危机。已知“C13”是指原子核内含有6个质子、7个中子的碳原子,则“He3”所指的氦原子原子核内含有( )
A.3个质子,没有中子 B.3个中子,没有质子
C.1个质子,2个中子 D.2个质子,1个中子
答案:D 解析:本题是一道信息题,由“C13”原子核内含有6个质子、7个中子可知,其中13是质子数与中子数之和。因氦原子的质子数为2,则其中子数应为3-2=1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com