
题目列表(包括答案和解析)
11.以NA代表阿伏加德罗常数,则下列关于热化学方程式:
 2C2H2(g)+5O2(g) 4CO2(g)
+2H2O(1) △H=-2600kJ·mol-1的说法,正确的是( )
2C2H2(g)+5O2(g) 4CO2(g)
+2H2O(1) △H=-2600kJ·mol-1的说法,正确的是( )
A.有10NA个电子转移时,该反应吸收1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量 C.有4NA个碳氧共同电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共同电子对生成时,放出1300kJ的能量
10.下列说法正确的是( )
A.凡是放热反应都是自发的,吸热反应都是非自发的;
B.自发反应一定是熵增大,非自发反应一定是熵减少或不变;
C.自发反应在任何条件下都能实现。
D.自发反应在恰当条件下才能实现;
9.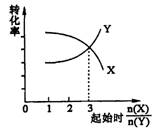 在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应,平衡后测得X、Y的转化率与起始时两物质的物质的量之比
在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应,平衡后测得X、Y的转化率与起始时两物质的物质的量之比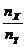 的关系如图所示,则X,Y的反应方程式可表示为( )
的关系如图所示,则X,Y的反应方程式可表示为( )
A.2X+Y 3Z B.3X+2Y
3Z B.3X+2Y 2Z
2Z
C.X+3Y Z D.3X+Y
Z D.3X+Y 2Z
2Z
8.液氨与水相似,存在着微弱的电离:2NH3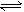 NH4++NH2-。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是( )
NH4++NH2-。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是( )
A.此温度下,液氨的离子积等于1×10-30
B.在液氨中放人NaNH2,则液氨的离子积数值将增大
C.此温度下,在液氨中加人NaNH2,则液氨中c(NH4+)<1×10-15mol/L
D.在液氨中加入NH4Cl,则液氨中c(NH4+)将大于c(NH2-)
7.下列不能减慢锌与稀盐酸的反应速率的措施是( )
A.降低温度 B.加入氯化钠溶液
C.加入少量CH3COONa固体 D.增大锌的用量
6. 将常温下pH=12的氢氧化钠溶液与pH=2的硫酸溶液分别加热,溶液PH的变化是( )
A.前者减少后者不变 B.前者减小后者增大 C.都不变 D.都减小
5. 有三支试管,分别加入下列物质后
甲:10mL 0.01mol·L-1 FeCl3溶液 和10 mL 0.01 mol·L-1 KSCN溶液
乙:5mL水10mL 0.01mol·L-1 FeCl3溶液 5mL 0.01mol·L-1 KSCN溶液
丙:10mL 0.1mol·L-1 FeCl3溶液 和10mL 0.1mol·L-1 KSCN溶液
观察这三支试管的颜色,其中颜色最浅的是( )
A.甲试管 B.乙试管 C.丙试管 D.无法判断
4.沼气是一种能源,它的主要成分是CH4。0.5molCH4完全燃烧生成CO2气体和液体H2O时,
放出445kJ热量,则下列热化学方程式中正确的是( )
A、CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ·mol-1
B、CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=+890kJ·mol-1
C、CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ·mol-1
D、1/2CH4(g)+O2(g)= 1/2CO2(g)+H2O(l) △H=-890kJ·mol-1
3.已知:H2(g)+F2(g)== 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ热量
2.关于强、弱电解质的叙述不正确的是( )
A.强电解质在溶液中完全电离,不存在电离平衡
B.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱
C.同一弱电解质同浓度的溶液,温度不同时,导电能力不同
D.强电解质在固态或液态时,可能不导电
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com