
题目列表(包括答案和解析)
2.2003年诺贝尔化学奖授予两位美国科学家,其中一位是阿格雷(Pete Agre),表彰他最先发现并表征了细胞膜上的水通道蛋白质,并把这种蛋白质暂命名为:CHIP28,下列关于CHIP28的说法中正确的是( )
A.这种蛋白质为人工合成的高分子化合物
B.这种蛋白质遇到HgCl2的浓溶液将发生盐析
C.这种蛋白质能完全水解生成单糖分子
D.这种蛋白质分子中存在“-CONH-”的结构
1.如今人们把食品分为绿色食品、蓝色食品、白色食品等类型。绿色植物通过光合作用转化的食品叫绿色食品;而直接从海洋获取的食品叫蓝色食品;通过微生物发酵制得的食品叫白色食品。下面属于白色食品的是
A.食醋 B.面粉 C.海带 D.食盐
25.(8分)芳香族化合物A和B的相对分子质量都小于200,完全燃烧时只生成CO2和H2O。B中碳、氢元素总的质量分数为65.2%。1 mol A水解生成 1 mol醋酸和 1 mol B。A溶液具有酸性,但遇FeCl3溶液不显色。
(1)A与B相对分子质量之差为 。
(2)一个B分子中应有 个氧原子。
(3)A的分子式为 ______ 。
(4)B的可能的三种结构简式是 。
贵州省清华实验学校09-10学年高二上学期12月月考
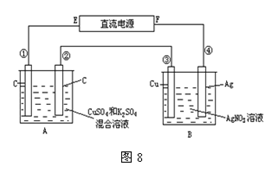
24.(6分)如图8所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,求通电前A池中原混合溶液Cu2+的浓度。
23.
|

|

 (提示CH3COO
(提示CH3COO CH3COONa +
CH3COONa + ONa)
ONa)

(1)写出E的结构简式
(2)A有2种可能结构,写出其结构简式
(3)写出F在浓H2SO4(170℃)作用下发生反应的化学方程式:
,反应类型 。
(4)写出F与H在加热和浓H2SO4催化作用下发生反应的化学方程式:
,反应类型 。
(5)在B、C、D、F、G、I化合物中,互为同系物的是 。
22.(8分)已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如图6(部分反应的条件、生成物被略去):
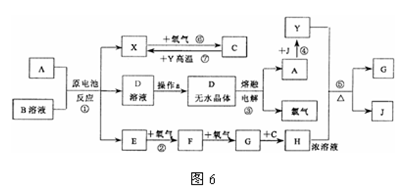
请填写下列空白:
⑴金属A为 ;操作a是将D溶液在HCl气流中蒸干,原因是
⑵反应②的化学方程式为: ;
反应⑤的化学方程式为: 。
⑶原电池反应①中,正极反应式为: 。
21. (6分)一定温度下,向如图5所示的带有可移动活塞的密闭容器中充入2 L
SO2 和1 L O2 的混合气体,发生如下反应2 SO2 (g) + O2 (g) 2 SO3
(g) 。
(6分)一定温度下,向如图5所示的带有可移动活塞的密闭容器中充入2 L
SO2 和1 L O2 的混合气体,发生如下反应2 SO2 (g) + O2 (g) 2 SO3
(g) 。
(1)若活塞可自由移动,平衡后,活塞停止在“2.1”处,容器内,
 V(SO3)=_____________L;该反应中SO2 的转化率为________。
V(SO3)=_____________L;该反应中SO2 的转化率为________。
(2)若开始时,充入容器的起始物质分别是①2 L SO2 和1 L O2 ;
②2 L SO3 (g) 和 1 L N2 ;③1 L SO2 、1 L O2 和 1 L SO3 (g),
使活塞固定在“3”处,达到平衡后,容器中SO3 (g)的体积分数大
小关系是 (用序号和“<”、“=”、“>”表示)。
(3)向(1)平衡后的容器中充入0.2 mol 的SO3,活塞移动后再次达到
平衡时,测得此过程中从外界共吸收了1.96 kJ 的热量,写出SO2 发生氧化反应的热化学方程式:________
20.(4分)对于弱酸在一定温度下达到电离平衡时,各粒子的浓度存在一种定量的关系。若在25℃时有HA H++A-,则K=C(H+)•C(A-)/ C(HA),式中K为电离平衡常数,只与温度有关,各粒子的浓度为达到平衡时的浓度。下表是几种常见弱酸的电离平衡常数(25℃)
H++A-,则K=C(H+)•C(A-)/ C(HA),式中K为电离平衡常数,只与温度有关,各粒子的浓度为达到平衡时的浓度。下表是几种常见弱酸的电离平衡常数(25℃)
|
酸 |
电离方程式 |
电离平衡常数 |
|
CH3COOH |
CH3COOH
 CH3COO-+H+ CH3COO-+H+ |
1.76×10-5 |
|
H2CO3 |
H2CO3  HCO3-+ H+ HCO3-+ H+HCO3-  CO32-+ H+ CO32-+ H+ |
K1=4.31×10-7 K2=5.61×10-11 |
|
H2S |
H2S  HS-+ H+ HS-+ H+HS-  S2-+ H+ S2-+ H+ |
K1=9.1×10-8 K2=1.1×10-12 |
|
H3PO4 |
H3PO4  H2PO4- + H+ H2PO4- + H+H2PO4-  HPO42-+ H+ HPO42-+ H+HPO42-  PO43-+ H+ PO43-+ H+ |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
回答下列问题:
(1)K只与温度有关,当温度升高时,K值 (填“增大”、“减小”或“不变”)
(2)在温度相同时,各弱酸K值不同,那么K值的大小与酸性相对强弱的关系是
(3)若把CH3COOH、 H2CO3 、HCO3-、H2S、 HS-、H3PO4 、H2PO4-、HPO42-都看作是酸,其中酸性最强的是 ,最弱的是
(4)电离平衡常数是用实验的方法测定出来的,现已经测得25℃时Cmol/L的CH3COOH的电离度为α(当若电解质在溶液里达到电离平衡时,溶液中已电离的电解质分子占原来总分子数的百分数叫做该电解质的电离度)。试表示该温度下醋酸的电离平衡常数K=
19.(4分)将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。问题1:化学变化过程中的平衡状态可以通过改变反应条件而发生变化。对电离平衡、水解平衡、化学平衡等各种平衡移动的方向与外界条件变化的关系请你运用一句话进行总结:_________________________________________________________。
问题2:1840年盖斯根据一系列实验事实得出规律:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O2(g)=CO2(g):△H=-395.41kJ/mol,C(石墨、s)+O2(g)=CO2(g):△H=-393.51kJ/mol,则金刚石转化石墨时的热化学方程式为:________ ____ ___。
18.(9分)电镀厂曾采用有氰电镀工艺,处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用图4装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率。

将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200 mL(其中CN-的浓度为0.05 mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
⑴甲中反应的离子方程式为 ,
乙中反应的离子方程式为 。
⑵乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等。丙中加入的除杂试剂是饱和食盐水,其作用是 ,丁在实验中的作用是 ,装有碱石灰的干燥管的作用是 。
⑶戊中盛有含Ca(OH)2 0.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于 。该测得值与工业实际处理的百分率相比总是偏低,简要说明可能的原因 。请提出一个能提高准确度的建议(要有可操作性,且操作简单) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com