
题目列表(包括答案和解析)
32.(19分)25°时,将0.01molCH3COONa和0.002molHCl溶于水,形成1L混合溶液:
(1)该溶液中存在三个平衡体系,用电离方程式或离子方程式表示:
①________________________;
②________________________;
③________________________。
(2)溶液中共有___种不同的粒子(指分子或离子)。
(3)在这些粒子中,浓度为0.01mol/L的是__,浓度为0.002mol/L的是__。
(4)__和__两种粒子物质的量之和等于0.01mol。
31.(9分)水的电离平衡曲线如下图所示。
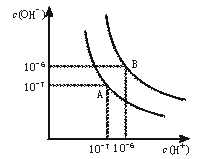 (1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
增加到
。
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
增加到
。
(2)将常温下的pH=8的Ba(OH)2溶液与常温下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。
(3)已知AnBm的离子积=[c(Am+)]n·[c(Bn-)]m?,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度。在某温度下,Ca(OH)2的溶解度为0.74 g,其饱和溶液密度设为1 g/mL,其离子积为 。
30.(18分)
(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铁水溶液呈 性 ,原因是(用离子方程式表示):
_____________________ _____________________________ 。把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的 。
20. .某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是 ( )

19.氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
A. 1mol/L甲酸溶液的pH约为3
B. HCN易溶于水
C. 10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应
D. 在相同条件下,HCN溶液的导电性比强酸溶液的弱
12.向等体积、pH=2的两种一元酸HA和HB的溶液中加入足量的镁粉,充分反应后,收集到H2的体积V(HA)> V(HB),下列说法正确的是
(A)HA一定是弱酸
(B)HB一定是强酸
(C)NaA溶液的碱性弱于NaB溶液的碱性
(D)反应开始时二者生成H2的速率相同
11.室温下,pH相同,体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
(A)加水稀释2倍后,两溶液的pH均减小
(B)使温度都升高20℃后,两溶液的pH均不变
(C)加适量的醋酸钠晶体后,两溶液的pH均增大
(D)加足量的锌充分反应后,醋酸产生的氢气比盐酸多
10.下列各方程式中,属于水解反应的是 ( )
A. 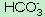 +H2O
+H2O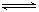 H2CO3+OH- B.
H2CO3+OH- B. 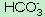 +H2O
+H2O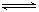 CO2-3+H3O+
CO2-3+H3O+
C.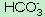 +OH-
+OH-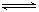 CO2-3+H2O D. CO2-3+H+=
CO2-3+H2O D. CO2-3+H+=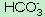
9. PH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的体积比是
A 11:1 B 9:1 C 1:11 D 1:9
7下列溶液一定现中性的是( )
A、PH=7的溶液 B、c(H+)=10-7mol/L的溶液
C、c(H+)= c(OH-)=3.5×10-7mol/L的溶液 D、酸碱恰好完全中和的溶液
8.
下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com