
题目列表(包括答案和解析)
2.鲨鱼是世界上惟一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。已知角鲨烯分子中含有30个碳原子及6个双键且不含环状结构,则其分子式为
A C30H60 B C30H56 C C30H52 D C30H50
1.下列物质中,不属于高分子化合物的是
A 花生油 B 棉花 C 淀粉 D 橡胶
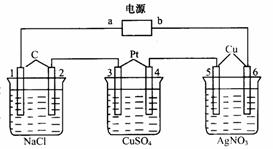
37、如下图所示:通电5min后,电极6质量减小1.28g,试回答下列问题:
(1)电源:a 极 ,C为 池
A池阴极反应:
A池阳极反应:---------------------
A池总反应离子方程式:
(2)若B槽中共收集到224mL气体(标况),且溶液体积为200mL(设电解过程中溶液体积不变),则通电前溶液中的Cu2+物质的量浓度为 。
(3)若A池溶液体积为200mL,且电解过程中溶液体积不变,则电解后,溶液pH为 。
36、常温下将0.01 mol CH3COONa和0.004 mol HCl溶于水,配成0.5 L混合溶液,请判断:
(1)溶液中共有 种粒子;
(2)溶液中有两种微粒的物质的量之和一定等于0.01 mol,他们是 和 ;
(3)溶液中nCH3COO- + nOH- --- nH+=
35、今有①CH3COOH ②HCl ③H2SO4三种溶液,用序号回答下列问题:
(1)当它们PH相同时,其物质的量浓度由大到小的排列顺序是 ;
(2)当它们的物质的量浓度相同时,溶液中CH+由大到小的排列顺序是 ;
(3)中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为 = ,① = 2 ;
(4)体积和浓度相同的①、②、③三种溶液,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积关系为 = , ② =
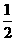 。
。
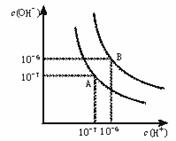
34.水的电离平衡曲线如下图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升高 到100℃时,水的电离平衡状态到B点,则此时水的离子积变为 。
(2)将100℃ 、pH=8的Ba(OH)2溶液与相同温度下pH=5的稀盐酸混合,并保持恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。
33. (1)氯化铝水溶液呈 (填“酸”、“中”或“碱”)性 ,原因是(用离子方程式表示):__________________________________________________ 。把AlCl3溶液蒸干,灼烧,最后得到的固体产物是 (填“化学式”)。
(2)在配制硫化钠溶液时,为了抑制水解,可以加入少量的 (填化学式);其水解的离子方程式为 。
32. 电子表和电子计算器常用微型银-锌原电池作电源,其电极分别为Ag2O和Zn,电解质溶液为
KOH溶液,电池总反应式为: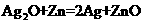 。
。
(1)若其中一个电极的电极反应式为 ,则该电极为 极 (填“正”或“负”),另一个电极的电极反应式为
.
,则该电极为 极 (填“正”或“负”),另一个电极的电极反应式为
.
(2)工作时,电池负极区溶液pH值 (填“增大”、“减小”或“不变”),电流由 (填“Zn”或“Ag2O”)极经外电路流向另一极。电路中每转移l mol电子,消耗Ag2O的物质的量
为 mol。
31、2006年1月12日美国升空的探测器在7月4日与彗星相撞,产生4.5吨TNT当量爆炸威力。其火箭推进剂仍然以肼(N2H4)作为主要燃料,NO2为氧化剂,反应生成N2和水蒸气。已知N2(g)+2O2(g)= 2NO2(g);ΔH= +67.7KJ/mol, N2H4(g)+O2(g)=N2(g)+2H2O (g);ΔH= -534KJ/mol。则肼和NO2反应的热化学方程式是___________ .
30.有关右图装置中的叙述正确的是( )
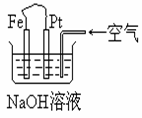 A.这是电解NaOH溶液的装置
A.这是电解NaOH溶液的装置
B.这是一个原电池装置,利用该装置可长时间的观察到
Fe(OH)2 沉淀的颜色
C.Pt为正极,其电极反应为:O2+2H2O +4e-=4OH-
D.Fe为阳极,其电极反应为:Fe-2e-+2OH-=2Fe(OH)2
第Ⅱ卷(非选择题,共40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com