
题目列表(包括答案和解析)
18.向含有FeCl3、BaCl2的酸性溶液中通入足量的SO2,有白色沉淀生成,过滤,向滤液中滴入KSCN溶液时,无明显现象,由此得出的正确结论是 ( )
A.白色沉淀是BaSO3
B.白色沉淀是BaSO4 k+s-5#u 
C.白色沉淀是BaSO3、BaSO4的混合物
D.FeCl3全部被SO2还原为FeCl2
17.某原电池总反应的离子方程式:2Fe3++Fe=3Fe2+不能实现该原理反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液
B.正极为C,负极为Fe,电解质溶液为Fe(NO3)2溶液
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3溶液
16.某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a,将其全部投入50mL b mol ·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是 ( )
A.若金属有剩余,在溶液中再滴人硫酸后,金属又开始溶解
B.若金属全部溶解,则溶液中一定含有Fe3+ k+s-5#u 
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:

15.燃料电池是燃料(CH4、H2、CO)与O2反应,以KOH(aq)为电解质溶液,将化学能转化为电能装置如图。下列有关H2的燃料电池的说法错误的是 ( )
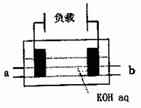 A.a处通入的气体是O2,b处通入气体是H2
A.a处通入的气体是O2,b处通入气体是H2
B.电池工作时,OH-向负极千移
C.负极反应为H2+2OH--2e-=2H2O
D.为了保持溶液浓度不变,需不断蒸
发水,不必补充KOH
14.在FeCl3、CuCl2混合溶液中,加入一定理的铁屑,反应完全后将固体滤出,下列说法中正确的是 ( )
A.若滤出的固体中只有铜,则溶液中一定含有阳离子是Fe2+,一定不含Cu2+
B.若滤出的固体中含铁和铜,则溶液中一定含有阳离子是Fe2+,一定不含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有阳离子是Fe2+,可能含有Cu2+
D.若滤出的固体中只有铜,则溶液中一定含有阳离子是Cu2+和Fe2+,一定不含Fe3+
13.向20mL2mol/LAlCl3溶液中加入30mLNaOH溶液,充分反应后得到0.78g沉淀,则NaOH溶液的物质的量浓度是 ( )
A.1mol/L B.2mol/L C.5mol/L D.8mol/L
12.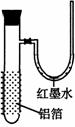 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),
将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久
铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断
下列说法错误的是 ( )
A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属,
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
11.铝在人体内积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为“食品污染源之一”而加以控制,铝在下列使用场合须加以控制的是 ( )
①糖果、香烟包装 ②电线、电缆
③牙膏皮 ④治疗胃酸过多的Al(OH)3药片
⑤用明矾净水 ⑥用明矾和小苏打昆合物作食品的膨化剂
⑦制造餐具与炊具 ⑧制造防锈漆k+s-5#u

A.②③④⑤⑥ B.①③④⑤⑥⑦ C.②③④⑤⑥⑦⑧ D.全部
10.下列叙述正确的是 ( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速度;
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀;k+s-5#u

③铜锌原电池工作时,铜片附近有大量气泡产生;
④构成原电池正极和负极的材料必须是两种金属;
⑤钢铁表面易锈蚀生成Fe2O3·nH2O
A.①②③④⑤ B.①③⑤ C.①②③⑤ D.②④
9.向含1molKAl(SO4)2的溶液中加入适量的Ba(OH)2溶液,使SO2-4沉淀完全,此时Al(OH)3沉淀的物质的量是 ( )
A.0mol B.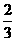 mol C.1mol D.1.33mol
mol C.1mol D.1.33mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com