
题目列表(包括答案和解析)
3.用物质的量都是0.1mol的CH3COOH和CH3COONa混合后配成1L溶液,已知溶液中的c(CH3COO-)>c(Na+),下列关系正确的是 ( )
A.c(H+)<c(OH-)
B.c(CH3COOH)>c(CH3COO-) k+s-5#u

C.c(CH3COO-)+c(OH-)=0.1mol•L-1 k+s-5#u

D.c(CH3COOH)+c(CH3COO-)=0.2mol•L-1
2.下列过程或现象与盐类水解无关的是 ( )
A.纯碱溶液去油污
B.铁在潮湿的环境下生锈k+s-5#u

C.加热氯化铁溶液颜色变深 D.浓硫化钠溶液有臭味k+s-5#u

1.下列纯净物中含有自由移动的Cl-离子的是 ( )
A.NaCl溶液 B.熔融的NaCl k+s-5#u 
C.液态HCl D.KClO3溶液 k+s-5#u 
26.(12分)钢铁工业是国家工业的基础。2006年我国粗钢产量突破4亿吨,居世界首位。某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工艺流程有了全面的感性认识。请您对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的
NaOH 溶液,充分反应后,过滤、洗涤、灼烧得4.80gFe2O3 。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2 气体224mL(标准状况)。k+s-5#u 
①计算此钢样粉末中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末分别加到100mL相同浓度的H2SO4 溶液中,充分反应后,测得的实验数据如下表所示:
|
实验序号 |
I |
II |
III |
|
加入钢样粉末的质量/g |
2.812 |
5.624 |
8.436 |
|
生成气体的体积/L(标准状况) |
1.120 |
2.240 |
2.800 |
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?
25.(10分)(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应: ;
银片上发生的电极反应: 。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后
称重,总质量为47g,试计算:
①产生氢气的体积(标准状况);
②通过导线的电量。(已知NA = 6.02×1023/mol,电子电荷为1.60×10-19C)
24.(12分)某混合粉末里可能含有明矾、纯碱、硝酸镁中的一种或几种,用下图所示的方法处理
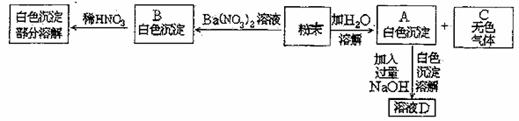
由此可得出结论:(用化学式回答)
①混合粉末由 组成
②B沉淀的成分是
③A沉淀是
,C气体是
k+s-5#u

④溶液D的主要成分是
⑤生成白色沉淀A和无色气体C的离子方程式是
23.(10分)已知某混合金属粉末,除铝处还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1:该混合金属粉末中除铝外还含有 元素;
假设2:该混合金属粉末中除铝外还含有 元素;
假设3:该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案k+s-5#u

基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
[提示]Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超过答题卡空间。
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
|
|
|
|
 21.(3分)已知某溶液中含Fe3+、Al3+共0.1mol,逐
21.(3分)已知某溶液中含Fe3+、Al3+共0.1mol,逐
渐滴入3mol/LnaOH溶液得到沉淀的量如图所示。
则此溶液中Fe3+和Al3+的物质的量之比为:
22.(3分)把ag铁铝合金粉末溶于足量盐酸中,加
入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、
灼烧,得到红棕色粉末的质量仍为ag,则原合金
中铁的质量分数为
20.某学生在实验室做了如下5个实验:
(1)在铝盐溶液中逐滴加入稀氨水直至过量
(2)在明矾溶液中加入NaOH溶液直至过量k+s-5#u

(3)在强碱性溶液中逐滴加入铝盐溶液直至过量
(4)在偏铝酸钠溶液中通入CO2直至过量
(5)在强酸溶液中加入偏铝酸钠溶液直至过量
根据以上实验画出下图的5个图象(纵坐标为沉淀物质的量,横坐标为溶液中加入物质的物质的量)实验与图象对立关系正确的是: ( )
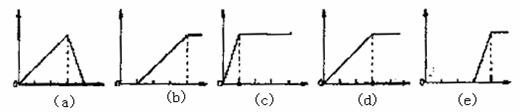
A.(1)和(a) B.(2)和(b) C.(3)和(e) D.(4)和(d)
第Ⅱ卷(非选择题,共50分)
19.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
( )
A.60mL B.45mL C.30mL D.15mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com