
题目列表(包括答案和解析)
23.(15分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4+ +6HCHO = 3H+ +6H2O + (CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当,然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤Ⅱ 将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。k+s-5#u

步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。k+s-5#u 
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数 (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察
。k+s-5#u 
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化k+s-5#u 
④滴定达到终点时,酚酞指示剂由 色变成
色。 k+s-5#u

(2)滴定结果如下表所示:
|
滴定次数 |
待测溶液的体积 |
标准溶液的体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 |
1.02 |
21.03 |
|
2 |
25.00 |
2.00 |
21.99 |
|
3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1010 mol ·L-1,则该样品中氮的质量分数为 。
22.(4分)某温度下在密闭容器中发生如下反应: 2M(g)+N(g)  2E(g)
2E(g)
若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为 ;平衡时的压强与起始时压强之比 。
21.(7分)将一元酸HA的溶液与一元碱BOH的溶液等体积混合,所得溶液呈酸性。
(1)若混合前酸、碱pH之和等于14,则HA一定是 酸,BOH 碱(填强或弱);溶液中水的电离程度:混合溶液 纯水(用“>、<、=”符号连接)
(2)若混合前酸、碱物质的量浓度相同,则HA一定是 酸,BOH 碱(填强或弱)溶液中水的电离程度:混合溶液 纯水 ,纯水 BOH溶液(用“>、<、=”符号连接)
20.(4分)pH值相同的 ①HCl溶液、②H2SO4溶液、③ CH3COOH溶液各100 mL
(1)分别用0.1 mol/L的NaOH 溶液中和,其中消耗NaOH 溶液最多的是 。
(用“>、<、=”符号连接V①、V②、V③,或n①、 n②、n③完成(2)题的填空)
(2)若加入足量的锌粉:反应开始时,反应速率 ;反应过程中,反应速率 ;反应结束时,生成气体的物质的量 .
19.(10分)有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测:
(1)该学生的操作是 (填“正确”或“错误”,其理由是 ;
(2)如不正确请说明理由,同时请分析是否一定有误差? ;
(3)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是 ,原因是 ;
(4)只从下列试剂中选择实验所需的试剂,你能否区分的0.1mol/L硫酸溶液和0.01mol/L硫酸溶液,简述操作过程 。k+s-5#u

试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液
D.蒸馏水 E.氯化钡溶液 F.pH试纸
18.某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。据图判断正确的是 ( )
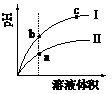
A.II为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点KW的数值比c点KW的数值大k+s-5#u

D.b点酸的总浓度大于a点酸的总浓度
第Ⅱ卷(非选择题,共46分)
17.根据以下事实得出的判断一定正确的是 ( )
A.HA的酸性比HB的强,则HA溶液pH比HB溶液的小
B.A+和B-的电子层结构相同,则A原子的核电荷数比B原子的大k+s-5#u

C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
16.磷钨酸H3PW12O40等杂多酸可代替浓硫酸用于乙酸乙酯的制备。下列说法不正确的是
( )
A.H3PW12O40在该酯化反应中起催化剂的作用
B.杂多酸盐Na2HPW12O40与Na3PW12O40都是强电解质
C.H3PW12O40、KH2PW12O40与Na3PW12O40含有相同的原子团k+s-5#u 
D.硅钨酸H4SiW12O40也是一种杂多酸,其中W的化合价为+8
15.下列情况下,一定能在溶液中同时大量共存的离子组是 ( )
A.由水电离出的 [H+] = 10-14 mol/L 的溶液中: Na+、HCO3-、Cl-、SO42-
B.PH试纸呈现红色的溶液: Fe2+、K+、NO3-、Na+
C.CO32-可以大量共存的溶液: Ag+、K+、NO3-、Al3+
D.PH = 2 的溶液中: SO42-、K+、NO3-、Al3+ k+s-5#u

14.已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH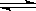 CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
A.加少量烧碱溶液 B.升高温度
C.加少量冰醋酸 D.加水k+s-5#u

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com