
题目列表(包括答案和解析)
10、 567.85 2N2H4(g)+2NO2(g) 3N2 (g)+4H2O(g) △H=-1135.7 kJ·mol-1
567.85 2N2H4(g)+2NO2(g) 3N2 (g)+4H2O(g) △H=-1135.7 kJ·mol-1
2、(1)化学式 聚集状态 气 液 固 oq
(2)温度 温度 焓变 温 度 反应物
(3)kJ·mol-1 J·mol-1
(4)系数 数值 物质的量 符号 数值
[基础训练]
1-5 A C D B C 6-9 CD CD BD A
(2)能量
2、(1)产物总焓-反应物的总焓
(2)△H=H(产物)-H(反应物)
(3)大于 吸收 吸热 小于 放出 放热
(4)一步 几步 焓变
2、(1)量热计 内 外 外 保温 内 温度 温度
(2)热容 kJ·k-1 温度 Q=-C(T2-T1) kJ kJ
12、0.3moL的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态B2O3和液态水,放出649.5kJ的热量,其热化学方程式为
又已知H2O(1)=H2O(g) △H=44kJ·moL-1则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量为 。
寒假作业第一课时 化学反应的热效应
11、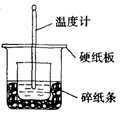 50mL0.5mol·L-1盐酸与50mL0.55mol·L-1NaOH
50mL0.5mol·L-1盐酸与50mL0.55mol·L-1NaOH
溶液在如图所示的装置中进行中和反应。通过测定反
应过程中所放出的热量可计算中和热,完成下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品
是 。
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬板纸,求得中和热数值 (填“偏大”“偏小”或“无影响”)。
(4)实验中改用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”),简述理由 。
|
10、 发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
试计算1mol肼和二氧化氮完全反应时放出的热量为 kJ,写出肼与二氧化氮反应的热化学方程式 。
9、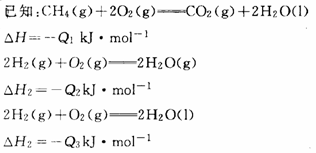
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复室温,则放出的热量为( )

8、下列关于△H(焓变)的说法正确的是( )
A.在任何条件下,化学反应的焓变都等于化学反应的反应热
B.△H>0时,反应吸收热量;△H<0时,反应放出热量
C.热化学方程式中△H的值与物质前的化学计量数无关
|
7、下列说法正确的是( )
A.需要加热方能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.反应是吸热还是放热必须看反应物和生成物所具有的总能量的相对大小
D.吸热反应在一定条件下也能发生
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com