
题目列表(包括答案和解析)
6.关于化学反应与能量的说法正确的是
A、中和反应是吸热反应 B、燃烧属于放热反应
C、化学键断裂放出能量 D、反应物总能量与生成物总能量一定相等
5.下列金属冶炼的反应原理,错误的是
A、2NaCl(熔融)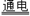 2Na+Cl2↑ B、MgO+H2
2Na+Cl2↑ B、MgO+H2 Mg+H2O
Mg+H2O
C、Fe3O4+4CO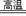 3Fe+4CO2
D、2HgO
3Fe+4CO2
D、2HgO 2Hg+O2↑
2Hg+O2↑
4.我国卫生部于2008年9月发布了“受三聚氰胺污染三鹿牌婴幼儿配方奶粉事件”。三聚氰胺是一种低毒性化工产品,婴幼儿大量摄入会引起泌尿系统疾患。下列描述属于三聚氰胺化学性质的是
A、三聚氰胺为白色晶体 B、快速加热会升华
C、常温下溶解度小,溶于热水[
D、在一般情况下较稳定,但在高温下可能会分解生成氰化物
3.“善待地球--科学发展。”下列行为中不符合这一主题的是
A、发展循环经济,构建资源节约型社会
B、加高工厂的烟囱,使烟尘和废气远离地表,减少污染
C、减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D、采用“绿色化学”工艺,建立环境友好型化工体系
2.设阿伏加德罗常数为6.02×1023 mol-1 。关于1 mol SO2的叙述正确的是
A、含有1 mol O2 B、含有6.02×1023个SO2分子
C、质量为64 g·mol-1 D、该物质的体积为22.4 L
1.下列变化属于物理变化的是
A、煤的干馏 B、油脂硬化 C、石油裂化 D、石油分馏
26、(11分)用滴定的方法来测定盐酸的浓度,实验数据如下所示:
|
实验序号 |
待测盐酸溶液的体积(m L) |
滴入0.40mol/L碳酸钠溶液的的体积(mL) |
|
1 |
20.0 |
22.9 |
|
2 |
20.0 |
23.1 |
|
3 |
20.0 |
24.8 |
|
4 |
20.0 |
22.8 |
|
5 |
20.0 |
23.2 |
(1)滴定中误差较大的是 次实验,造成这种误差的三个可能原因是:
① ;
② ;
③ 。
(2) 计算未知盐酸的浓度(数据精确到0.1) 。
25、(10分)在一个固定容积的密闭容器中,保持一定的温度进行以下反应: H2(g)+Br2(g) 2HBr(g)已知加入1 mol H2和2 mol Br2时,达到平衡后生成
2HBr(g)已知加入1 mol H2和2 mol Br2时,达到平衡后生成
a mol HBr(见下表已知项),在相同条件下,且保持平衡时各组分的体积分数不变,对下列编号①-③的状态,填写下表中的空白。
|
已知 编号 |
起始状态时物质的量n(mol) |
平衡状态时HBr物质的量n(mol) |
||
|
H2 |
Br2 |
HBr |
||
|
1 |
2 |
0 |
a |
|
|
1 |
2 |
4 |
0 |
|
|
2 |
|
|
1 |
0.5a |
|
3 |
m |
g(g≥2m) |
|
|
24、(5分)在10 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)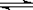 CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
|
t/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答:
(1)该反应为________(填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K =________________。
(3)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO) = 0.0080 mol/L ,则CO2的转化率为______________。
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 _________℃
23、(5分)常温下,两种溶液① 0.1 mol/L NH3·H2O ② 0.1 mol/L NH4Cl中:
(1)溶液①的pH __________7(填“>”、“<”或“=”),其原因是
(用电离方程式表示)。
(2)溶液②呈________ 性(填“酸”、“碱”或“中”)。水解反应是吸热反应,升温可以____(填“促进”或“抑制”)NH4Cl 的水解。
(3)下列关于两种溶液中c(NH4+) 的叙述正确的是 ___________(填字母)。
a.两种溶液中c(NH4+) 都等于0.1 mol/L
b.两种溶液中c(NH4+) 都小于0.1 mol/L
c.NH4Cl溶液中c(NH4+) 小于NH3·H2O溶液中c(NH4+)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com