
题目列表(包括答案和解析)
8.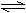 一定量混合气体在密闭容器中发生如下反应:aA(g)+bB(g)
cC(g),该反应达到平衡后,测得A气体的浓度为0.5mol/L。在恒温下将该密闭容器的容积扩大到原来的2倍,再次达到平衡时,测得A的浓度为0.3mol/L,则下列叙述正确的是
一定量混合气体在密闭容器中发生如下反应:aA(g)+bB(g)
cC(g),该反应达到平衡后,测得A气体的浓度为0.5mol/L。在恒温下将该密闭容器的容积扩大到原来的2倍,再次达到平衡时,测得A的浓度为0.3mol/L,则下列叙述正确的是
A.平衡向正反应方向移动 B. a+b <c
C.B的转化率提高 D.C的体积分数降低
7.将等物质的量的镁铝混合后,平均分成四等分,分别加入到足量的下列溶液中,充分反应后放出H2最多的是
A.18mol/L H2SO4 B.4mol/L HNO3 C.3mol/L HCl D.8mol/LNaOH
6.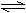 对于反应N2 (g)+ 3H2(g) 2NH3(g)(正反应为放热反应)的平衡体系,在其它条件不变时,采取下列措施不能使正、逆反应速率都增大的是
对于反应N2 (g)+ 3H2(g) 2NH3(g)(正反应为放热反应)的平衡体系,在其它条件不变时,采取下列措施不能使正、逆反应速率都增大的是
A.减小NH3的浓度 B.升高温度 C.加入铁触媒 D.增大体系压强
5.若使0.1mol/L醋酸溶液的电离程度和pH值均增大,应采取的措施是
A.加水 B.加盐酸 C.加醋酸钠 D.加热
4.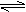 当反应2SO2+O2 2SO3达到平衡后,通入18O2,再次达到平衡时,18O存在于
当反应2SO2+O2 2SO3达到平衡后,通入18O2,再次达到平衡时,18O存在于
A.SO3、O2 B.SO2、SO3 C.SO2、O2 D.SO2、SO3、O2
3.常温下,物质的量浓度相同的下列溶液,NH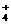 浓度最大的是
浓度最大的是
A.NH4Cl B.NH4HSO4 C.CH3COONH4 D.NH4HCO3
2.已知反应4NH3+5O2 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则下列正确的关系是
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则下列正确的关系是
A.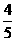 v(NH3)=v (O2) B.
v(NH3)=v (O2) B.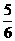 v(O2)=v(H2O)
v(O2)=v(H2O)
C.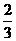 v(NH3)=v(H2O) D.
v(NH3)=v(H2O) D.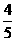 v(O2)=v(NO)
v(O2)=v(NO)
1.有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,把滴定管中的溶液全部流下排出,承接在量筒中,量筒内溶液的体积
A.大于40.0mL B.为40.0 mL C.大于10.0mL D.为10.0mL
32、(6分)将1L 2mol∕L HCl溶液与足量AgNO3溶液充分反应。试计算:
(1)生成AgCl的物质的量为多少?
31、(8分)在化学课上,围绕不活泼金属能否与硝酸反应,进行了如下实验探究:在两支试管中各放入一小块铜片,分别加入稀硝酸和浓硝酸,立即塞上带导管的胶塞,并将导管通入另一只盛有NaOH溶液的试管中。
请回答:
(1)实验中观察到,其中一支试管中反应较缓慢,产生的一种无色气体是 (填化学式)。
(2)另一支试管中反应剧烈,产生的一种红棕色气体是 (填化学式),
写出产生该气体的化学方程式: 。
(3)根据上述实验现象,表明硝酸具有 (填序号)。
①酸性 ②不稳定性 ③强氧化性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com