
题目列表(包括答案和解析)
13.已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO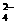 .某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中不正确的是
.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中不正确的是
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
12.下列关于电解质溶液的叙述正确的是
A.常温下,NH4Cl与某物质的混合溶液pH<7,则其组成可能是NH4Cl与HCl或NH4Cl与NH3•H2O
B.将pH=5的氢氟酸溶液稀释后,溶液中所有离子的浓度均降低
C.常温下,同浓度的Na2S与NaHS溶液中所含的粒子种类相同
D.将一元酸HA溶液与一元碱BOH溶液等体积混合,若所得溶液呈酸性,则混合溶液中离子浓度一定满足:c(B+)>c(A-)>c(H+)>c(OH-)
11.有甲、乙两瓶醋酸稀溶液,测得甲的pH=a,乙的pH=a+1.下列推断正确的是
A.物质的量浓度c(甲)是c(乙)的10倍
B.溶液中的c(OH-)甲是乙的10倍
C.由水电离产生的c(H+)乙是甲的10倍
D.与等量的NaOH反应消耗甲、乙两酸的体积V(乙)>10V(甲)
10. 室温下,某无色透明溶液中由水电离出来的H+和OH-浓度的乘积为1×10-24,则此溶液中可能大量共存的离子组为
室温下,某无色透明溶液中由水电离出来的H+和OH-浓度的乘积为1×10-24,则此溶液中可能大量共存的离子组为
A.HCO3-、Al3+、Na+、SO42- B.I-、NO3-、K+、NH4+
C.MnO4-、Cl-、SO42-、K+ D.SiO32-、SO32-、Na+、Cl-
9.下列电离方程式中正确的是
A.Na2HPO4溶于水:Na2HPO4=2Na++H++PO43-
B.NaHSO4熔化:NaHSO4=Na++H++SO42-
C.HF溶于少量水:2HF = H++HF2一
D.(NH4)2Fe(SO4)2溶于水:(NH4)2Fe(SO4)2=2NH4++Fe2++2SO42一
8.( )下列实验操作或对实验事实的叙述正确的是
①.用碱式滴定管量取20.00 mL 0.1000 mol·L-1 KMnO4溶液;②.某无色溶液的焰色反应呈黄色,则该溶液是钠盐溶液;③.配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;④.用稀硝酸清洗做过银镜反应实验的试管;⑤.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;⑥.用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;⑦.某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+.
A.①⑤⑦ B. ②③④⑦ C. ③④⑦ D.②③⑤⑥
7.( )已知25 ℃ 时,AgCl 的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大()
B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出.
D.将AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,因为AgCl溶解度大于AgI
6.( )在一支25mL的酸式滴定管中盛入0.1mol/L HCl溶液,其液面恰好在5mL刻度处.若把滴定管内溶液全部放入烧杯中,再用0.1mol/L NaOH溶液进行中和,则所需NaOH溶液的体积
A.大于20mL B.小于20mL C.等于20mL D.等于5mL
5.( )从植物花中可提取一种简写为HIn的有机物,它在水溶液中因存在下列平衡:
HIn(aq,红色)  H+(aq)+In-(aq,黄色) 而用作酸碱指示剂.往该溶液中加入Na2O2粉末,则溶液颜色为()
H+(aq)+In-(aq,黄色) 而用作酸碱指示剂.往该溶液中加入Na2O2粉末,则溶液颜色为()
A.红色变深 B.不变化 C.黄色变深 D.褪为无色
4.( )等体积、等物质的量浓度的NaCl和NaF溶液中,阴阳离子总数相比
 A.前者多 B.后者多 C.一样多 D.无法判断
A.前者多 B.后者多 C.一样多 D.无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com