
题目列表(包括答案和解析)
7.从化学反应速率和化学平衡两方面考虑,合成氨应采用的条件是 ( )
 低温、高压、催化剂
低温、高压、催化剂  低温、低压、催化剂
低温、低压、催化剂
 高温、高压、催化剂
高温、高压、催化剂  适当温度、高压、催化剂
适当温度、高压、催化剂
6.能确认化学平衡状态发生了移动的是 ( )
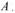 化学反应速率发生了改变
化学反应速率发生了改变
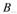 有气态物质参加的可逆反应达到平衡后,改变了压强
有气态物质参加的可逆反应达到平衡后,改变了压强
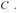 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
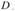 可逆反应达到平衡后,使用催化剂
可逆反应达到平衡后,使用催化剂
5. 在C(s)+CO2(g) 2CO(g)反应中,可使反应速率增大的措施是 ( )
在C(s)+CO2(g) 2CO(g)反应中,可使反应速率增大的措施是 ( )
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
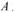 ①②③④
①②③④ 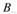 ②③④⑤
②③④⑤  ①②③
①②③ 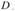 ②③④
②③④
4.下列说法正确的是 ( )
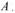 增大压强,活化分子数增加,化学反应速率一定增大
增大压强,活化分子数增加,化学反应速率一定增大
 升高温度,活化分子百分数增加,化学反应速率不一定增大
升高温度,活化分子百分数增加,化学反应速率不一定增大
 活化分子间所发生的碰撞为有效碰撞
活化分子间所发生的碰撞为有效碰撞
 加入催化剂,使活化分子百分数大大增加,化学反应速率大大加快
加入催化剂,使活化分子百分数大大增加,化学反应速率大大加快
3.氨与重水(D2O)形成的碱与盐酸反应,这一反应生成的盐在溶液中电离生成的阳离子的化学式是( )
 NH3D+
NH3D+ 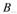 NH2D2+
NH2D2+ 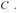 ND3H+
ND3H+ 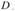 NH4+
NH4+
2.某氮的氧化物和一氧化碳在催化剂的作用下充分反应,生成氮气和二氧化碳,若测得氮气和二氧化碳的物质的量之比为1∶2,则该氮的氧化物是 ( )
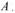 N2O
N2O 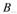 NO
NO 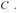 NO2
NO2 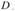 N2O5
N2O5
1.砷为第四周期VA族元素,根据其在元素周期表中的位置推测,砷不可能具有的性质是 ( )
①砷原子比磷原子核外多一个电子层,共多8个电子 ②砷酸H3ASO4是一种氧化性强酸
③砷能表现出一定的金属性 ④砷难与H2化合,砷化氢极不稳定 ⑤砷在通常状况下是固
体 ⑥可以有-3、+3、+5等多种化合价 ⑦AS2O5对应水化物的酸性比H3PO4弱
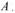 ①⑥
①⑥ 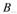 ①②
①② 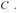 ④⑥⑦
④⑥⑦ 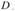 ③⑤
③⑤
(二)测定铝合金中的铝的百分含量
①取该样品a克,将样品溶于足量的稀盐酸中,过滤;
②在滤液中加入过量的氢氧化钠溶液,过滤;
③往第②步的滤液中通入足量的CO2,过滤,将沉淀用蒸馏水洗涤后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为b克。
回答下列问题:
(1)在第①步操作中溶解所使用的玻璃仪器为玻璃棒、 ,滤液中主要含有Mg2+、Na+、 和Cl-离子;
(2)在第②步操作中氢氧化钠溶液需要过量的原因是 ,写出该步骤中生成沉淀的离子方程式
(3)第③步灼烧过程中可在下列哪种仪器中进行
A.烧杯 B.试管 C.坩埚 D.蒸发皿
(4)第③步灼烧后得到的固体是
(5)合金中铝的质量分数是



(一)探究铝合金的抗腐蚀性能
①向一只小烧杯里加入20mL0.5mol/LCuSO4溶液,把一小块铝合金浸入溶液中,1-2分钟后将铝片取出,观察铝片表面的现象
②取1只试管,加入10mL2mol/LNaOH溶液,将一块铝片放入NaOH溶液里,片刻取出后,用蒸馏水冲洗后浸入CuSO4溶液里。1-2分钟后将铝片取出,观察铝片表面的现象
实验①铝片没有变化,实验②铝片表面的现象是
发生此现象的原因是
32.(4分)为了达到下表中的实验要求,请选择合适的化学试剂及实验方法,将其标号填入对应的空格中。
|
实验目的 |
|
||
|
测定某废水的pH |
|
||
|
检验早晨的自来水是否含Cl2分子 |
|
||
|
对蛋白质溶液进行分离提纯 |
|
||
|
检验胃舒平是否含有碳酸氢钠 |
|
33.(12分)某铝合金中含有镁、铜、硅,为了测定研究它的抗腐蚀性能和测定合金中铝的含量,某研究性学习小组设计了如下实验:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com