
题目列表(包括答案和解析)
23. 一定温度下,有a、盐酸;b、硫酸;c、醋酸三种酸的稀溶液。(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是_______________ ;
②当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序为 ;
③将c(H+)相同的三种酸均稀释10倍,pH由大到小的顺序为_____________
22. 物质的量浓度相同的 ① 氨水 ② 氯化铵 ③ 碳酸氢铵 ④ 硫酸氢铵
⑤硫酸铵 五种溶液中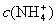 大小的顺序是__________________
大小的顺序是__________________
21.(4分)0.1mol/L的下列溶液:
①HCl、②CH3COOH、③CH3COONa、④NaOH、⑤FeCl3、⑥NaCl 。
(1)pH由小到大排列顺序为 (填序号);
(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
20.下列混合溶液中,各离子浓度的大小顺序正确的是 ( )
A. 10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合,
c(Clˉ) > c(NH4+)> c(OHˉ) > c(H+)
B. 10mL0.1mol/LNH4 Cl溶液与5mL0.2mol/LNaOH溶液混合,
c(Na+)= c(Clˉ)> c(OHˉ) > c(H+)
C. 10mL0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合,
c(Na+)= c(CH3COOˉ)> c(OHˉ) > c(H+)
D. 10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合,
c(Cl-) > c(Na+)> c(OH-ˉ) > c(H+)
第II卷(非选择题 ,共50分)
19.下列各组中的比值等于2:1的是 ( ) A. pH为12的烧碱溶液与Ba(OH)2溶液的物质的量浓度之比
B. K2S溶液中c(K+)与c(S2-)之比
C. 相同温度下0.2mol/L醋酸溶液与0.1mol/L醋酸溶液中的c(H+)之比
D.10mL0.5mol/L的盐酸与5mL0.5mol/L的盐酸溶液中的c(H+)之比
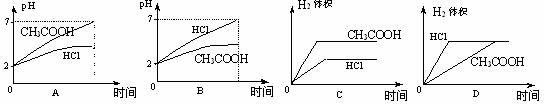
18.在体积均为1 L,pH均等于2的盐酸和醋酸溶液中,分别投入0.23 gNa,则图中比较符合反应事实的曲线是 ( )
17.工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)=Si(s)+4HCl(g);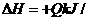 mol(Q>0)
mol(Q>0)
某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C. 反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L.min)
D. 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
16.下列事实能说明醋酸是弱酸的是 ( )
①当温度低于16.6℃时醋酸可凝结成冰一样晶体 ②0.1 mol/L的醋酸钠溶液的pH约为9 ③等体积等物质的量浓度的硫酸比醋酸消耗氢氧化钠多 ④0.1mol/L的醋酸的pH值约为4.8 ⑤pH都等于4且等体积的醋酸和盐酸,与等浓度NaOH溶液充分反应时,醋酸液消耗碱液多[来
A. ②④⑤ B. ②④ C. ②③④ D. ②③
15.高温下,某反应达平衡,平衡常数K=。恒容时,温度升高,H2 浓度减
小。下列说法正确的是 ( )
A. 该反应的焓变为正值 B. 恒温恒容下,增大压强,H2浓度一定减小
C. 升高温度,逆反应速率减小
D. 该反应化学方程式为CO + H2O 催化剂高温 CO2 + H2
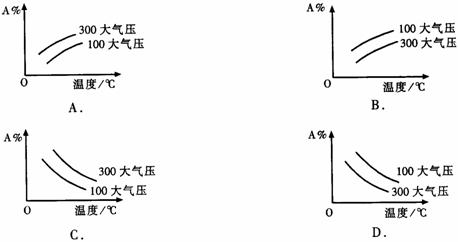
14.在可逆反应mA(g)+nB(g)  pC(g) △H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t、压强P关系正确的是 ( )
pC(g) △H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t、压强P关系正确的是 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com