
题目列表(包括答案和解析)
5. 在下列平衡2CrO42-(黄色)+2H+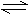 Cr2O72-(橙红色)+H2O中,溶液颜色介于黄和橙红色之间,今欲使溶液的橙红色加深,则要在溶液中加入 ( )
Cr2O72-(橙红色)+H2O中,溶液颜色介于黄和橙红色之间,今欲使溶液的橙红色加深,则要在溶液中加入 ( )
A、H+ B、OH- C、K+ D、H2O
4. 对于反应:A+B=C下列条件的改变一定能使化学反应速率加快的是( )
A、增加A的物质的量 B、升高体系的温度
C、增加体系的压强 D、减少C的物质的量浓度
3. 1gH2燃烧生成液态水放出142.9KJ的热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g)=2H2O(l) ΔH=-142.9kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
C. 2H2+O2=2H2O ΔH=-571.6kJ·mol-1
D. H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8kJ·mol-1
2. 一定条件下反应N2(g)+3H2(g)
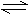 2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为( )
2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为( )
A.1.2mol/(L·min) B.1mol/(L·min) C.0.6mol/(L·min) D.0.4mol/(L·min)
1.下列反应中,生成物的总能量大于反应物总能量的是( )
A.氢气在氧气中燃烧 B.氢气与氯气化合
C.中和反应 D.焦炭在高温下与水蒸气反应
28.(11分)某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度(选填大于、小于或等于) 25℃,其理由是
。
若将此温度下pH=11的苛性钠溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比:
(1)若所得混合液为中性,则a:b= ;此溶液中各种离子的浓度由大到小排列顺序是 。
(2)若所得混合液的pH=2,则a:b= ;此溶液中各种离子的浓度由大到小排列顺序是 。
27.(9分)(1)一种一元强酸HA溶液中加入一种碱MOH后,溶液呈中性,则A-与M+物质的量浓度的大小关系为:c(A-) c(M+)。(填“=”、“<”、“>”、“无法判断”等)
(2)等体积等浓度的MOH强碱溶液和HA弱酸溶液混合后,混合溶液中的各离子浓度的大小关系为:
(3)在物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa混和溶液中,测得c(Na+)<c(CH3COO-),则c(CH3COO-)+c(CH3COOH) 0.02mol/L(填“=”、“<”、“>”等),水溶液的酸碱性为 (填“酸性”、“碱性”、“中性”、“无法判断”)
(4)常温下,0.lmol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是
。
(用离子方程式和必要的文字说明)。
26.(6分)已知(1)Cu2+、Fe2+在pH为 4-5的条件下不水解,这一条件下Fe3+几乎全部水解。
(2)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O。
现用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液的过程如下:[
①取50 mL纯净的盐酸,加入一定量的粗CuO加热搅拌、充分反应后过滤,测知滤液的pH=3。
②向滤液中加入双氧水、搅拌。 ③调节②中溶液的pH至4,过滤。
④把③所得滤液浓缩。
回答以下问题:(1)②中发生反应的离子方程式是 。
(2)③中使pH升高到4,采取的措施是:加入过量的 并微热、搅拌。
A. NaOH B. 氨水 C. CuCl2 D. CuO
(3) ③中过滤后滤渣的成分是
25.(8分)在一固定容积的密闭容器中,保持一定条件下进行以下反应:
X(气)+2Y(气)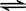 3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为 。
(2)在相同实验条件下,若在同一容器中改为加入2 mol X和8 mol Y,若要求在反应混合气体中Z体积分数不变,则还需加入Z mol。
(3)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加
入 mol Y, mol Z,才能使平衡时Z为0.9a mol。
24.(4分)(1)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。放出571.6kJ的热量,表示H2燃烧热的热化学方程式为
。 (2)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com