
题目列表(包括答案和解析)
25.(8分)在一固定容积的密闭容器中,保持一定温度,在一定条件下进行反应:
A(g)+2B(g) 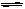 3C(g),已知加入1molA和3molB且达平衡后生成a molC,问:
3C(g),已知加入1molA和3molB且达平衡后生成a molC,问:
⑴平衡时C在反应混合气体中的体积分数是 (用字母a表示)。
⑵在相同实验条件下,若在同一容器中改为加入2molA和6molB,达平衡时C在反应混合气中的体积分数____________ (填增大、减少或不变)。
⑶在相同实验条件下,若在同一容器中改为加入2molA和8molB,若要求平衡后C在反应混合气中的体积分数不变,则还应加入C mol。
⑷ 在同一容器中加入n molA和3n molB,在平衡时C的物质的量为mmol,若改变实验条件,可以使C的物质的量在m~2m之间变化,那么n与m的关系应是____________
(用字母m、n表示)。
24.(8分)在一定条件下,xA + yB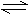 zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白:
⑴若A、B、C都是气体,减压后向逆反应方向移动,则x、y、x之间的关系是 。
⑵已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向 方向移动,且A、B的状态中至少有一种是
⑶加热后C的百分含量减少,则正反应是 反应(选填“吸热”、“放热”)。
23.(6分)在一小烧杯里混合10ml 0.01mol/L FeC13溶液和10ml 0.01mol/L KSCN溶液,溶液立即变为红色。
⑴写出反应的化学方程式: 。
⑵再向溶液中滴入1mol/LFeC13溶液,现象 ,平衡向 反应方向移动,KSCN浓度会 。
⑶在烧杯中加入KC1固体,颜色 。(填变深、变浅或不变)
22.(6分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如右图所示,由图中数据分析:
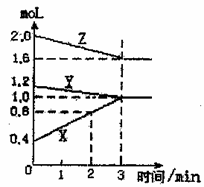 ⑴该反应的化学方程式可表示为
,
⑴该反应的化学方程式可表示为
,
⑵反应开始至2分钟末,X的反应速率为:
。
⑶该反应是由 _________ 开始反应的(填正反应、逆反应或正逆反应同时)。
21. 某温度下,纯水中c(H+)=3.0×10-7 mol/L,则此时c (OH-)= ;
温度不变,向水中滴入盐酸使c(H+)=3.0 mol/L,则溶液中c (OH-)= 。
20.(2分) 在250C、101KPa时,1克甲醇(CH30H)完全燃烧生成CO2和液态水时放热22.68KJ,则能表示甲醇燃烧热的热化学方程式为:
19.(2分)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现已知火箭发射时可用肼(N2H4)为燃料,以NO2作氧化剂,反应生成N2(g)和气态的水,据下列的2个热化学反应方程式:
N2(g)+2O2(g)= 2NO2(g) △H= +67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+ 2H2O(g) △H= -534kJ/mol
试写出肼(N2H4)与NO2反应生成N2(g)和气态的水的热化学反应方程式:
18. 在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡CH3COOH CH3COO-+H+ 对于该平衡,下列叙述正确的是(
)
CH3COO-+H+ 对于该平衡,下列叙述正确的是(
)
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
第II卷(非选择题 ,共46分)
17. 一定条件下向一带活塞的密闭容器中充入2molSO2和1molO2,发生如下反应:
2SO2(g)
+O2(g) 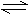 2SO3(g) 达平衡后改变下列条件,SO3气体的平衡浓度不改变的是( )
2SO3(g) 达平衡后改变下列条件,SO3气体的平衡浓度不改变的是( )
A.保持温度和容器的体积不变,充入1molSO2(g)
B.保持温度和容器内压强不变,充入1molAr(g)
C.保持温度和容器内压强不变,充入1molO2(g)
D.保持温度和容器内压强不变,充入1molSO3(g)
16. 在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) 1/2N2(g)+CO2(g)ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
1/2N2(g)+CO2(g)ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度 B .加催化剂同时增大压强
C.升高温度同时充入N2 D .降低温度同时增大压强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com