
题目列表(包括答案和解析)
2.(8分)现有下列4种有机物:
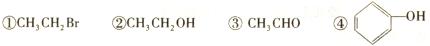
(1)能与浓溴水反应生成白色沉淀的是____________(填序号,下同),能发生银镜反应的是
___________,能发生水解反应的是_________。
(2)②发生消去反应的化学方程式是____________________。
1.(4分)现有下列5种有机物:

(1)其中符合通式CnH2n+2的是_______(填序号,下同),与①互为同分异构体的是_________,与③互为同系物的是____________。
(2)用系统命名法给⑤命名,其名称为__________。
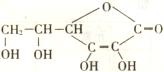
2.(6分)维生素c又称为抗坏血酸,在人体内有重要功能。
已知其结构简式如右图所示:请回答:
(1)维生素C的分子式为___________。若将___________
(填水果或蔬菜名称)切碎捣烂,加水溶解提取其滤液,就能达到充分提取水果中的维生素C的目的,这也说明维生素C_____________(填“能”或“不能”)溶于水。
(2)某同学在实验室探究维生素C的性质。在试管中取少量淀粉溶液,滴加几滴稀碘水,观察到溶液变为_________色,再向试管中滴入维生素C的溶液,发现原溶液颜色逐渐变浅。该实验说明维生素C具有____________性。
(3)该同学继续探究维生素C在(2)中表现的性质,可选择的试剂是___________(填序号)。
①KI溶液 ②酸性KMnO4溶液
 《有机化学基础》模块试题
《有机化学基础》模块试题
《化学与生活》模块试题
1.(4分)下表是某食品包装上的部分说明。
|
品名 |
油炸方便面面饼 |
|
配料 |
①小麦粉
②食盐 ③精炼棕榈油 ④栀子黄等 |
|
保质期 |
六个月 |
|
生产日期 |
见封口 |
 上表所列配料中,属于着色剂的是______(填序号,下同),属于调味剂的是______,富含油脂的是___________,富含淀粉的是___________。
上表所列配料中,属于着色剂的是______(填序号,下同),属于调味剂的是______,富含油脂的是___________,富含淀粉的是___________。
6.(8分)现有A、B、X、Y、Z五种短周期元素,原子序数依次增大。它们的性质或原子结构如下表:
|
元素 |
性质或原子结构 |
|
A |
原子核内只有一个质子 |
|
B |
单质是空气中含量最多的气体 |
|
X |
原子的最外层电子数是次外层电子数的3倍 |
|
Y |
短周期元素中原子半径最大的元素 |
|
Z |
最高正化合价与最低负化合价的代数和为6 |
请回答:
(1)X元素在元素周期表中的位置是________________________。
(2)Z单质通入Y的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的离
子方程式为___________________________________________________________。
(3)化合物甲由A和B两种元素组成且质量比为3:14。甲与X单质在催化剂、加热条件下发生的反应是工业上制取硝酸的基础,写出该反应的化学方程式_______________。
(4)为证明Z单质的氧化性比Br2强,某同学设计如下实验。请完成下面实验报告。
|
实验操作 |
实验现象 |
结论及解释 |
|
①取少量NaBr溶液于试管中,滴加___________,振荡; ②再加入少量CCl4,振荡,静置 |
①溶液由无色变为橙黄色。 ②溶液分层,_____________ ____________________。 |
氧化性:Z单质>Br2>离子方程式____________________ _______________________。 |
5.(8分)某工厂的工业废水中含有Fe3+、Cu2+、 等离子,为了减少污染并变废为宝,工厂计划从该废水中回收金属铜并得到硫酸亚铁。生产流程如下图所示(所加试剂均为过量):
等离子,为了减少污染并变废为宝,工厂计划从该废水中回收金属铜并得到硫酸亚铁。生产流程如下图所示(所加试剂均为过量):
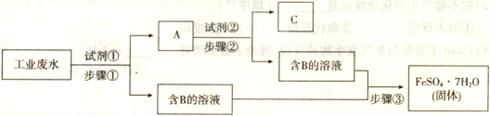
请回答:
(1)试剂①应该是___________,A中含有的物质是__________。步骤①中发生反应的离
子方程式为_________________________________________________________。
(2)步骤①、②中共同的分离提纯操作是___________________,步骤③中的操作是加热、
___________、冷却、结晶、过滤。
(3)某同学为了验证长期放置的FeSO4·7H2O固体是否变质,取少量该固体于试管中,加入少量蒸馏水使其溶解,再滴入几滴___________溶液,若观察到_______________
_________________,则证明该固体已经变质。
4.(4分)钠和铝两种金属的单质及其化合物在生产、生活中有着广泛的应用。请回答:
(1)两种金属中,能与冷水发生剧烈反应的是____________,由此说明,钠的金属性比铝
___________(填“强”或“弱”)。
(2)钠和铝的最高价氧化物对应水化物的碱性强弱比较____________>___________(填化
学式)。
(3)向氯化铝的溶液中逐滴加入NaOH溶液,先产生白色沉淀,后沉淀溶解,得到无色透明溶液。写出沉淀溶解时反应的离子方程式:
________________________________________________________________________。
3.(4分)现有下列四种物质:①SO2 ②NH3 ③Na2SO4溶液④Fe(OH)3胶体。其中加入氯化钡溶液产生白色沉淀的是__________(填序号,下同),能使品红溶液褪色,加热后恢复原来颜色的是______________,能使湿润的红色石蕊试纸变蓝的是_____________,当光束通过时,能观察到丁达尔效应的是_____________。
2.(3分)在①CH3CH2OH、②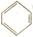 、③CH3COOH三种有机物中,家庭中可用于除水垢的是______________(填序号,下同),不溶于水的是____________,一定浓度的溶液可作为医用消毒剂的是_________。
、③CH3COOH三种有机物中,家庭中可用于除水垢的是______________(填序号,下同),不溶于水的是____________,一定浓度的溶液可作为医用消毒剂的是_________。
1.(3分)铜与稀硝酸可发生反应: (稀)
(稀)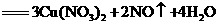 。
。
该反应中,作为氧化剂的物质是___________(填化学式),作为还原剂的物质是__________(填化学式);若反应中生成了l mol NO,则需消耗___________mol HNO3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com