
题目列表(包括答案和解析)
15.能正确表示下列反应的离子方程式是( )
A.硫酸铜溶液与氢氧化钡溶液反应 : Ba2+ + SO42― = BaSO4 ↓
B.氯化铝溶液中加入过量的氨水: Al3+ + 3NH3·H2O = Al(OH)3 ↓+ 3NH4
C.溴化亚铁溶液中通入足量的氯气:2Fe2+ + Cl2 = 2Fe3+ + 2Cl―
D.石灰石溶于醋酸:CaCO3 + 2H+ = Ca2+ + CO2 ↑+ H2O
14.某溶液中加入铝片有氢气产生,则该溶液中一定能大量共存的离子组是( )
A.Cl― NO3― Ba2+ Fe3+ B.SO42― S2― Al3+ Mg2+
C.Na+ K+ SO42― Cl― D. NH4+ Ba2+ Cl― HCO3―
13.盐酸、醋酸和碳酸氢钠是实验室里常见的药品。下列表述正确的是 ( )
A.NaHCO3溶液中:c(H+)+c(CO32-)=c(OH-)+c(H2CO3)
B.10 mL0.10mol·L-1 CH3COOH溶液加入10 mL0.10mol·L-1 NaOH溶液后,混合溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.在NaHCO3溶液中加入与其等体积等物质的量浓度的NaOH溶液后,混合溶液中的阴离子只有CO32-和OH-
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
12.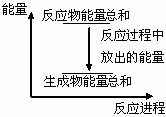 对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH<0 的化学反应,下列叙述不正确的是 ( )
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH<0 的化学反应,下列叙述不正确的是 ( )
A.反应过程中能量关系可用右图表示
B.ΔH的值与反应方程式的计量系数有关
C.若将该反应设计成原电池,锌为负极
D.若将其设计为原电池,当有32.5g锌溶解时,正极
放出气体一定为11.2L
11.下列对一些实验事实的理论解释正确的是 ( )
|
选项 |
实 验 事 实 |
理 论 解 释 |
|
A |
MgCl2溶液中加入浓氨水,出现白色沉淀 |
碱性:NH3·H2O
> Mg(OH)2 |
|
B |
用pH试纸测得CH3COONH4溶液的pH=7 |
CH3COONH4不能水解 |
|
C |
HF的沸点高于HCl |
HF分子间存在氢键,而HCl不存在 |
|
D |
将SO2通入氯水中,氯水褪色 |
SO2具有漂白性 |
10.发射“神七”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知:N2(g) + 2O2(g) = 2NO2(g) △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H = – 534.0kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是 ( )
A.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l) △H = – 1135.7kJ/mol
B.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g) △H = – 1000.3kJ/mol
C.N2H4(g) + NO2(g) = 3/2N2(g) + 2H2O(l) △H = – 1135.7kJ/mol
D.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g) △H = – 1135.7kJ/mol
9.下列关于实验现象的描述不正确的是 ( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌
C.将FeCl3溶液加热蒸发至干并灼烧,最后得到FeCl3晶体
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
8.某醋酸溶液的PH=a,某NaOH溶液的PH=b,又知a+b=14,若将上述溶液等体积混合后所得溶液显酸性,则所得溶液中各种离子浓度相对大小为 ( )
A. C(AC-) > C(Na+)>C(OH-)>C(H+) B. C(Na+)>C(AC-)> C(OH-) >C(H+)
C. C(AC-)> C(Na+) >C(H+) > C(OH-) D. C(Na+)>C(AC-)> C(H+) > C(OH-)
7.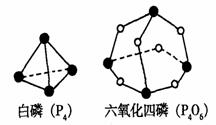 化学反应可视为旧键断裂和新键形成的过程。
化学反应可视为旧键断裂和新键形成的过程。
化学键的键能是形成(或拆开)1 mol化学键时
释放(或吸收)的能量。已知白磷(P4)和P4O6边的
分子结构如右图所示;现提供以下化学键的
键能:P-P 198KJ·mol-1、P-O 360kJ·mol-1、
O=O 498kJ·mol-1。则关于1mol P4和3mol O2
完全反应(P4+3O2==P4O6)的热效应说法正确的是 ( )
A.吸热1638 kJ B.放热1638 kJ
C.放热126 kJ D.吸热126 kJ
6.关于如图所示装置的叙述,正确的是 ( )
A.铜是阳极,铜片上有气泡产生
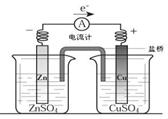 B.铜片质量逐渐减少
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com