
题目列表(包括答案和解析)
24、甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH___1(选填>,<,=)。简要说明pH试纸的使用方法: 。
(3)乙方案中,说明HA是弱电解质的现象是_________ 。
(4)乙方案的不足之处是
(5)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
23. (6分)某反应aA(g) + bB(g) cC(g) + dD(g),取a mol A和bmol B置于V L容器中,1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为
mol·L-1,C的浓度为
cC(g) + dD(g),取a mol A和bmol B置于V L容器中,1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为
mol·L-1,C的浓度为
mol·L-1,这段时间内反应的平均速率若以物质A的浓度变化来表示应为 。
22.(25℃)时有pH为a的盐酸和pH为b的NaOH溶液,取Va L该盐酸与该NaOH溶液中和,需Vb LNaOH溶液,问:
(1)若a+b=14,则Va/Vb= (填数字);
(2)若a+b=13,则Va/Vb= (填数字);
(3)若a+b>14,则Va/Vb= (填表达式)当a≤6, b≥8且a+b=14,则
Va Vb(填“<”、“>”或“=”)。
21. 1g乙醇完全燃烧生成液态水放出热量akJ,则乙醇燃烧热化学方程式为:
。
20. 室温下0.1mol·L-1NaOH溶液滴定amL某浓度的HCl溶液,达到终点时消耗NaOH溶液bmL,此时溶液中氢离子的浓度[H+]是( ) mol·L-1
A 0.1/(a+b) B 0.1b/(a+b) C 1×107 D 1×10-7
第Ⅱ卷(非选择题)
19. 在密闭容器中发生反应:aX(气)+bY(气)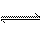 cZ(气)+dW(气)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是( )
cZ(气)+dW(气)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是( )
A.平衡向逆反应方向移动 B.a + b > c + d
C. Z的体积分数减小 D.X的转化率下降
18.一定条件下,在容积为2L的密闭容器里加入一定物质的量的A和B,发生如下反应并建立平衡: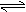 A(g) +
2B(g) C(g)+2D(g) 测得平衡时各物质的浓度是:[A]=0.3 mol/L,[B]=0.2
mol/L,[C]=0.15 mol/L。最初向容器里加入A的物质的量是( )
A(g) +
2B(g) C(g)+2D(g) 测得平衡时各物质的浓度是:[A]=0.3 mol/L,[B]=0.2
mol/L,[C]=0.15 mol/L。最初向容器里加入A的物质的量是( )
A 0.5 mol B 0.8 mol C 0.9 mol D 1.2 mol
17. 在一恒容的密闭容器中,A(g)+ B(g) C(g)的平衡体系中,若增大A的浓度而使平衡向右移动,当达到新的平衡时,则下列说法不正确的是( )
在一恒容的密闭容器中,A(g)+ B(g) C(g)的平衡体系中,若增大A的浓度而使平衡向右移动,当达到新的平衡时,则下列说法不正确的是( )
A.A的平衡浓度一定比原来平衡时大 B.B的平衡浓度一定比原来平衡时小
C.C的百分含量一定比原来平衡时大 D.A的转化率一定比原来平衡时大
16.将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c (NH4+) = c(Cl-) ⑤c (NH4+) < c(Cl-) 正确的是 ( )
A.①⑤ B.③④ C.②⑤ D.②④
15.能正确表示下列反应的离子方程式是( )
A、铜与浓硝酸反应:Cu+4H++2NO3-== Cu2++2NO2↑+2H2O
B、纯碱与水反应:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
C、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
D、硫酸氢钠与氢氧化钠溶液反应:H++OH-= H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com