
题目列表(包括答案和解析)
3.下列分子中,具有极性键的非极性分子是 ( )
A.NH3 B.H2O C.N2 D.CO2
2.关于晶体的下列说法正确的是 ( )
A.离子晶体中一定不含有非极性键
B.分子晶体中一定含有共价键
C.原子晶体的熔点一定比金属晶体高
D.晶体中只要有阴离子就一定有阳离子
1.在一定温度下,反应:2A(s)+2B(g)=======C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是 ( )
A.容器内的压强不随时间而变化B.混合气的密度不再随时间而变化
C.A的质量不再改变 D.平衡混合气的平均相对分子质量不再改变
29. 请在以下(1)、(2)两小题中任选一题作答,若两道题都做,则以第一道题为准。(5分)
(1)为测定一种复合氧化物型的磁性粉末材料的组成,称取6.26g样品,将其全部溶于过量稀硝酸后,配成100mL溶液。取50mL溶液,加入硫酸钾溶液,生成白色沉淀,经过过滤、洗涤、烘干后得2.33g固体。另取25mL溶液,加入少量硫氰化钾溶液,显红色。再取余下的25mL溶液,加入过量氢氧化钠溶液,生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得0.80g固体。请计算并结合推理,填写下表:
|
组成该磁性材料的元素是 |
|
|
各元素的质量比是[ m(x) |
: : = : : |
|
各元素的原子个数比是 n(x) |
: : = : : |
|
该磁性材料的化学式 |
|
|
用氧化物的形式表示 |
|
(2)400℃
,1.01×105Pa时,1.5L某烃蒸气能在aL氧气中完全燃烧,体积增大至(a+3)L(400℃
,1.01×105Pa测定)请回答:
①该烃在组成上必须满足的条件是 。
②当a=10L时,该烃可能的化学式为(最少写出三种)
。
③ 当该烃的化学式为C7H8时,
a的取值范围是 。
高&考%资(源#网
28.(5分)0.05mol某烃完全燃烧,生成二氧化碳气体5.6L(标准状况下)和5.4g水。
(1)通过计算写出该烃的分子式。
(2)若该烃的一氯代物只有一种结构,写出该烃的结构简式,并用系统命名法命名。
27.(10分)实验室制取乙烯的装置如下图④
,试回答:
(1)烧瓶中加入的两种试剂是 ;
(2)烧瓶中发生的化学反应其化学方程式是 。
(3)实验室制乙烯时,常因温度过高而发生副反应,请写出生成二氧化硫、二氧化碳和水蒸气的化学方程式 。
(4)请用下图中编号为①~④
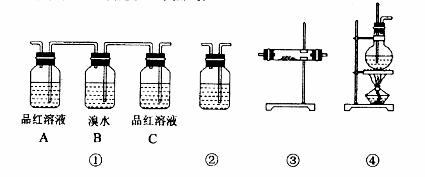 的实验装置,设计一个实验,以验证上述反应的混合气体中含有的二氧化硫、二氧化碳和水蒸气。
的实验装置,设计一个实验,以验证上述反应的混合气体中含有的二氧化硫、二氧化碳和水蒸气。
用装置的编号表示装置的连接顺序(按气体从左向右的流向):
→
→ → 。
(5)实验时装置①中A瓶中的现象是 ;结论是 ;B瓶的作用是 ;若C瓶中品红溶液不褪色,可得出的结论是
。
(6)装置③中加入的固体药品是 ;装置②中盛放的溶液是 。
26.(6分)除去下列物质中的杂质,请将所用试剂和分离操作的名称填入下表(括号中物质为杂质)
|
|
被提纯的物质 |
除杂所用的最佳试剂 |
分离操作名称 |
|
1 |
溴苯(Br2) |
|
|
|
2 |
C2H2(H2S) |
|
|
|
4 |
SiO2(Al2O3) |
|
|
25.(2分)有一种铁的氧化物样品Wg,加入140mL 5mol/L的盐酸恰好完全溶解,假设溶解过程中Fe2+没有被空气氧化成Fe3+,所得溶液还能吸收0.56L(标准状况下)氯气,恰好完全反应使其中的Fe2+ 全部转化为Fe3+ 。该样品的化学式为 。
24.(7分)提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据如图所示化学反应框图进行填空。
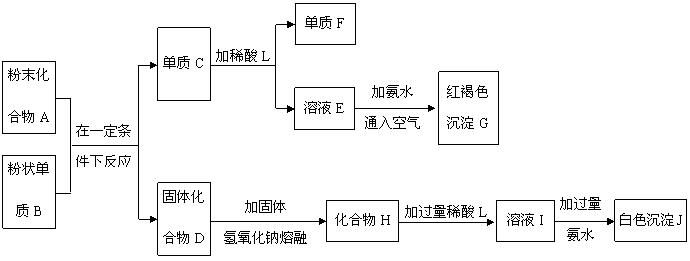
(1)单质B是 ;单质F是 。(写化学式)
(2)写出由E生成G化学反应的离子方程式和化学方程式
; ;
(3)溶液I中所含金属离子是 ;
(4)写出由I到J发生化学反应的离子方程式 ;
(5)若由C→
E+F改变用浓酸,则不能选用的浓酸是(写化学式) 。
23.(6分)乙烯的电子式为 ;它的同系物的通式为 ;相对分子质量为56的烃化学式为 ;其中为链状结构的烃的同分异构体结构简式分别为 ; ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com