
题目列表(包括答案和解析)
7.将pH=3的强酸溶液和pH=12的强碱溶液混合,当混合液的pH等于11时,强酸与强碱溶液的体积比是: ( )
A.10∶1 B.1∶9 C.9∶2 D.9∶1
6.将pH=3的盐酸与pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是( )
A.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
B.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
5.下列说法中正确的是 ( )
A.在25℃时,无论是酸性、碱性还是中性溶液中,其c(H+)和c(OH-)乘积都等于1×10-14
B.0.1mol/LNaOH溶液和0.1mol/L 氨水中,其c(OH-)相等
C.pH为3 的盐酸中,其c(H+)是pH为1 的盐酸中的3 倍
D.在Na3PO4溶液中,c(Na+)/c(PO43-)=3 / 1
3. 一定温度下,可逆反应2NO2((g)
一定温度下,可逆反应2NO2((g)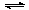 2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是:
2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
A.①④⑤⑥ B.①②③⑤ C.②③④⑥ D.以上全部

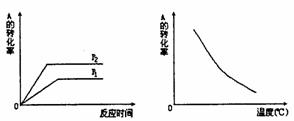 4.如图所示,可逆反应:mA(g)+nB(g) xC(g),在不同温度、压强下反应物A的转化率的变化情况。下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是 ( )
4.如图所示,可逆反应:mA(g)+nB(g) xC(g),在不同温度、压强下反应物A的转化率的变化情况。下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是 ( )
A.放热,m+n>x
B.放热,m+n<x
C.吸热,m+n<x
D.吸热,m+n>x
|
A.2-乙基-3,3-二甲基戊烷 CH3
B.3,3-二甲基-4-乙基戊烷 CH3-CH2- C- CH-CH3
C.3,3,4-三甲基己烷 CH3 C2H5
D.2,3,3-三甲基己烷
2.设NA表示阿伏加德罗常数,下列论述中不正确的是 ( )
A.18gNH4+含有的电子数为10NA
B.NA个H2SO4分子和NA个H3PO4分子的质量比为1:1
C.3.9gK变为K+时,失去的电子数为0.1NA
D.常温常压下,11.2LO2所含的氧原子数为NA
34、 (7分)(1)CaC2+2H2O→CH≡CH↑+Ca(OH)2 。
(7分)(1)CaC2+2H2O→CH≡CH↑+Ca(OH)2 。
(2)CH2=CH2 ,加成 (3)H2 ,CO2 (4)是
(5)略
37.(4分)Fe和CuSO4溶液反应,若反应后溶液的体积为1L,生成的铜的质量为32g。求:
(1)反应消耗的Fe的质量;
(2)反应后溶液中FeSO4的物质的量浓度。
36.(6分) 某溶液中可能含有Ag+、Al3+、Ba2+、Mg2+中的一种或几种。根据以下实验所得的现象,将适当的结论填入空格中。
(1) 向溶液中加入过量的盐酸,有白色沉淀生成。则肯定含有的离子是 。离子方程式是 ;
(2) 将(1)所得的溶液过滤后,往滤液中逐渐加入NaOH溶液,有白色沉淀生成,继续加入NaOH溶液,沉淀全部溶解,得到澄清溶液。则又可肯定含有的离子是 ,肯定不含的离子是 ;
(3) 在(2)所得的澄清溶液中加入Na2SO4溶液,产生白色沉淀。则肯定含有的离子是 ,离子方程式是 。
35.(5分) 下图是某学生设计的加热NaHCO3的装置图。试回答下列问题:
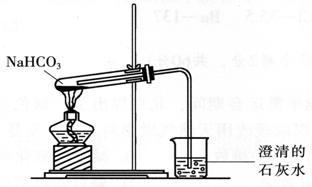 (1)烧杯内产生的现象是 。
(1)烧杯内产生的现象是 。
(2)图中有三处错误,它们是:
, 和 。
(3)请写出试管内发生反应的化学方程式
34.(7分)乙炔俗称电石气,是因为电石遇水可产生乙炔。乙炔可以制备一些简单有机化
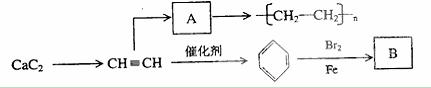 合物,其关系如图所示。 请按要求回答下列问题:
合物,其关系如图所示。 请按要求回答下列问题:
(1)写出用电石制备乙炔的化学反应方程式 ;
(2)A的结构简式为
,由 生成A的反应属于
反应;(填写反应类型)
生成A的反应属于
反应;(填写反应类型)
(3)实验室制取乙炔的装置,还可以用来制取哪些气体? , (任写两种即可);
(4)苯分子中的各原子是否处于同一平面内 (填“是”或“否”);
(5)写出苯与液溴在一定条件下发生反应生成B的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com