
题目列表(包括答案和解析)
16.在固定容积的密闭容器中按4:1的体积比通入CO2和H2的混合气体,加热到850℃时,建立下列平衡:CO2(g)+H2(g) CO(g)+H2O(g),在此温度下,平衡常数K=1,则反应达平衡时氢气转化率是
CO(g)+H2O(g),在此温度下,平衡常数K=1,则反应达平衡时氢气转化率是
A.50% B.80%
C.20% D.60%
永州市2009年下期期末质量检测试卷
15.在一定条件下,固定容积的密闭容器中反应:2NO2(g) 2NO(g)+O2(g),△H>0达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO(g)+O2(g),△H>0达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
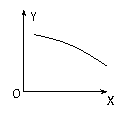 A.X表示温度时,Y表示NO2物质的量
A.X表示温度时,Y表示NO2物质的量
B.X表示压强时,Y表示NO2的含量
C.X表示反应时间时,Y表示混合气体的密度
D.X表示NO2物质的量,Y表示O2的物质的量
14.已知NaHSO4在水中的电离方程式为NaHSO4 =Na++H++SO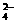 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液pH为2,对于该溶液,下列叙述不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液pH为2,对于该溶液,下列叙述不正确的是
A.该温度高于25℃
B.此溶液中,水电离出来的c(H+)=1.0×10―10 mol/L
C.此溶液中,水的离子积常数为KW=1.0×10―12
D.该温度下加入等体积pH值为12的NaOH溶液可使反应后的溶液恰好呈中性
13.钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2 ②4Fe(OH)2+O2+2H2O=4Fe(OH)3
③2Fe(OH)3=Fe2O3+3H2O
下列说法正确的是
A.反应①、②中电子转移数目相等
B.反应①中氧化剂是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
12.以碳棒为电极电解NaC1水溶液,下列叙述正确的是
A.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
B.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
C.电解时在阳极得到氯气,在阴极得到金属钠
D.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
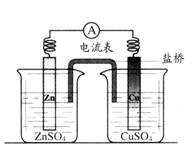
11.关于右图所示的原电池,下列说法正确的是
A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.锌电极发生还原反应,铜电极发生氧化反应
D.铜电极上发生的电极反应是2H2+2e-=H2↑
10. 往0.2L 0.1mol·L-1的NaOH溶液中通入224mL的CO2(标准状况),则下列关于所得溶液中的离子浓度关系,不正确的是
往0.2L 0.1mol·L-1的NaOH溶液中通入224mL的CO2(标准状况),则下列关于所得溶液中的离子浓度关系,不正确的是
A.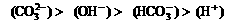
B.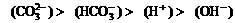
C.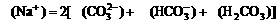
 D.
D.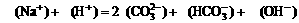
9. 已知31g白磷变成红磷放出18.39kJ热量,则下列两反应中:
4P(白、s)+5O2(g)=2P2O5(s),△H1
4P(红、s)+5O2(g)=2P2O5(s),△H2
△H 1和△H 2的关系是:
A.△H 1>△H 2 B.△H1=△H2
C.△H 1<△H 2 D.无法确定
8.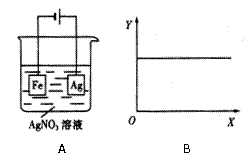 按A图装置进行实验,若图B的X轴表示流入电极的电子的量,则Y轴不可能表示的情况是
按A图装置进行实验,若图B的X轴表示流入电极的电子的量,则Y轴不可能表示的情况是
A.c(Ag+)
B.c(NO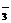 )
)
C.溶液的c (H+)
D.银棒质量
7.
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),ΔH<0,下列叙述正确的是
4NO(g)+6H2O(g),ΔH<0,下列叙述正确的是
A.达到化学平衡时,4υ正(O2)=5υ逆(NO )
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.达到平衡后,若升高温度,NH3的百分含量会减少
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com