
题目列表(包括答案和解析)
24..如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1mol时,下列说法正确的是( )
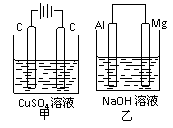
A.溶液的质量变化:甲减小乙增大
B.溶液pH值变化:甲减小乙增大
C.相同条件下产生气体的体积:V甲 = V乙
D.电极反应式:甲中阴极:Cu2++2e-=Cu,乙中负极:Mg-2e-= Mg2+
23.据最新研究表明:用于电动汽车的铝-空气燃料电池是以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B. 以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
22.为了测定苛性钾(KOH)的纯度,取样品0.56g,溶于水制成1L溶液,取此溶液25.00ml,用0.005 mol·Lˉ1硫酸标准溶液进行滴定消耗24.00ml时恰好完全反应(已知杂质都不和硫酸反应),则苛性钾的纯度为( )
A.96% B.48% C.9.6% D.56%
21.在蒸发皿中加热蒸干并灼烧下列物质的溶液,可以得到该物质的是( ) A.氯化铝 B.碳酸氢钠 C.硫酸镁 D.盐酸溶液
20.实验测得常温下0.1mol/L某一元酸(HA)溶液的pH值等于1,0.1mol/L某一元碱(BOH)溶液里C(H+)/(OH-)=10-12。将此两种溶液等体积混合后,所得溶液中的各离子的浓度由大到小排列的顺序是( )
A.C(B+)>C (A-)>C(OH-)>C(H+) B.C(A-)>C(B+)>C(H+)>C(OH- )
C.C(B+)=C(A-)>C(H+)=C(OH-) D.C(B+)>C(A-)>C(H+)>C(OH-)
19.下列说法正确的是( )
A.在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2·L-2
C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
D.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1 AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小
18.把分别盛有足量熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为 ( )
A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
17.下列离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.以石墨作电极电解氯化铝溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.AlCl3溶液中加入过量的浓氨水:Al3+ +4NH3•H2O == AlO2- + 4NH4+ + 2H2O
D.等体积、等浓度的稀溶液Ba(OH)2与NH4HCO3稀溶液混合:
Ba2+ +2OH- + NH4+ + HCO3- == BaCO3↓ + NH3•H2O + H2O
16.同体积的1 mol·Lˉ1的HCl、H2SO4、CH3COOH、HNO3分别加入过量的Mg;下列叙述中正确的是 ( )
A.HNO3、HCl、H2SO4中放出H2的速率相同
B.HCl、HNO3中放出H2的量相等
C.HCl、CH3COOH中放出H2的量相等
D.H2SO4中放出H2的量最多,其余的相等
15.中学阶段介绍的应用电解法制备的物质主要有三种:一是铝的工业制备;二是电解饱和NaCl溶液制备烧碱;三是金属钠的制备。下列关于这三个工业生产的描述中正确的是( )
A.电解法制铝时一般是用熔融态的氧化铝进行电解,但也可用其相应的盐如熔融态的 A1C13
B.电解法生产铝时,每转移3mol电子的时候,就能生产出1mol的铝。
C.在电解饱和NaCl溶液中,电解池中的阴极产生的是H2,NaOH在阳极附近产生
D.电解饱和NaCl溶液和金属钠的冶炼都用到了NaC1,在电解时它们的阴极都是C1-失电子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com