
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
20ЃЎЂХ ЯжгавЛЭИУїЕФзЂЩфЦїеыЭВЃЌГфТњNO2ЦјЬх(ШчЭММз)ЃЌЕБЭЦЖЏЛюШћЪБЃЌЦјЬхЕФбеЩЋНЋЁЁЁЁЁЁЁЁЁЁ (ЬюЁАБфЧГЁБЁЂЁАБфЩюЁБЁЂЁАЯШБфЩюКѓБфЧГЁБЛђЁАЯШБфЧГКѓБфЩюЁБ)ЃЌЕБЦјЬхЬхЛ§БфЮЊЭММзЕФвЛАыЪБ(ШчЭМвв)ЃЌNO2ЕФХЈЖШЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЭЦбЙЛюШћЧАNO2ХЈЖШЕФ2БЖЁЃЕБЙлВьЕНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЪБЃЌПЩШЗЖЈеыЭВФквбОДяЕНСЫЛЏбЇЦНКтзДЬЌЁЃЕБЛюШћКѓРЪБЃЌЭЈЙ§еыЭВгжЮќНјЩйСПNO2ЦјЬхЃЌдйЧАЭЦЛюШћЙЬЖЈдкЭМввЮЛжУЃЌNO2ЕФзЊЛЏТЪНЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЛђЁАВЛБфЁБ)ЁЃ

 ЁЁ
ЁЁ
ЂЦ СэгавЛЭИУїЕФзЂЩфЦїеыЭВЃЌГфТњH2ЁЂI2ЁЂHIЦјЬх(ШчЭММз)ЃЌЕБЭЦЖЏЛюШћЪБЃЌЦјЬхЕФбеЩЋНЋЁЁЁЁЁЁЁЁЁЁ (ЬюЁАБфЧГЁБЁЂЁАБфЩюЁБЁЂЁАЯШБфЩюКѓБфЧГЁБЛђЁАЯШБфЧГКѓБфЩюЁБ)ЃЌЕБЦјЬхЬхЛ§БфЮЊЭММзЕФвЛАыЪБ(ШчЭМввЃЌДЫЪБI2ШдЮЊЦјЬх)ЃЌHIЕФХЈЖШЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЭЦбЙЛюШћЧАHIХЈЖШЕФ2БЖЁЃ
19ЃЎКуЮТЯТЃЌНЋa mol N2гыb mol H2ЕФЛьКЯЦјЬхЭЈШывЛИіЙЬЖЈШнЛ§ЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃКN2 (g) + 3 H2(g) 2NH3(g)ЁЃ
2NH3(g)ЁЃ
(1)ШєЗДгІНјааЕНФГЪБПЬtЪБЃЌnt (N2)ЃН13molЃЌnt (NH3)ЃН6molЃЌМЦЫуaЕФжЕ
(2)ЗДгІДяЦНКтЪБЃЌЛьКЯЦјЬхЕФЬхЛ§ЮЊ716ЃЎ8L(БъПіЯТ)ЃЌЦфжаNH3ЕФКЌСП(ЬхЛ§ЗжЪ§)ЮЊ25%ЁЃМЦЫуЦНКтЪБNH3ЕФЮяжЪЕФСПЁЃ
(3)дЛьКЯЦјЬхгыЦНКтЛьКЯЦјЬхЕФзмЮяжЪЕФСПжЎБШ(аДГізюМђећЪ§БШЃЌЯТЭЌ)ЃЌn(ЪМ)ЁУn(ЦН) ЃНЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)дЛьКЯЦјЬхжаЃЌaЁУbЃН ЁЁЁЁЁЁЁЁ ЁЃ
(5)ДяЕНЦНКтЪБЃЌN2КЭH2ЕФзЊЛЏТЪжЎБШЃЌ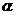 (N2)ЁУ
(N2)ЁУ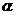 (H2)ЃНЁЁ ЁЁЁЁЁЁЁЁ ЁЃ
(H2)ЃНЁЁ ЁЁЁЁЁЁЁЁ ЁЃ
(6)ЦНКтЛьКЯЦјЬхжаЃЌn(N2)ЁУn(H2)ЁУn(NH3)ЃНЁЁ ЁЁЁЁЁЁ ЁЃ
18ЃЎдквЛЖЈЬхЛ§ЕФУмБеШнЦїжаЃЌНјааШчЯТЛЏбЇЗДгІЃК
CO2(g)+H2(g) CO(g)+H2O(g)ЃЌ
CO(g)+H2O(g)ЃЌ
ЦфЛЏбЇЦНКтГЃЪ§KКЭЮТЖШtЕФЙиЯЕШчЯТБэЃК
|
tЁц |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
ЛиД№ЯТСаЮЪЬтЃК
(1)ИУЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊK ЃНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ИУЗДгІЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЗДгІ(бЁЬюЮќШШЁЂЗХШШ)ЁЃ
(3)ФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЖрбЁПлЗж)ЁЃ
aЃЎШнЦїжабЙЧПВЛБфЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ bЃЎЛьКЯЦјЬхжа c(CO)ВЛБф
cЃЎІде§(H2)ЃНІдФц(H2O)ЁЁЁЁЁЁЁЁЁЁ dЃЎc(CO2)ЃНc(CO)
(4)ФГЮТЖШЯТЃЌЦНКтХЈЖШЗћКЯЯТЪНЃКc(CO2)ЁЄc(H2)ЃНc(CO)ЁЄc(H2O)ЃЌЪдХаЖЯДЫЪБЕФЮТЖШЮЊЁЁЁЁЁЁ ЁцЁЃ
17ЃЎЖдгкЗДгІ2A(g) + B(g) 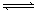 2C(g)дкЗДгІЙ§ГЬжаCЕФжЪСПЗжЪ§ЫцЮТЖШБфЛЏШчЭМЫљЪОЃЌЪдШЗЖЈЃК
2C(g)дкЗДгІЙ§ГЬжаCЕФжЪСПЗжЪ§ЫцЮТЖШБфЛЏШчЭМЫљЪОЃЌЪдШЗЖЈЃК
ЁЁ (1)T0ЖдгІЕФVе§гыVФцЕФЙиЯЕЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)е§ЗДгІЮЊЁЁЁЁЁЁЁЁ ЁЁШШЗДгІЁЃЁЁ
ЁЁ (3)AЁЂBСНЕуе§ЗДгІЫйТЪЕФДѓаЁЙиЯЕЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)ЮТЖШTЃМT0ЪБЃЌWcж№НЅдіДѓЕФдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
16ЃЎвбжЊtЁцЃЌp kPaЪБЃЌдкШнЛ§ЮЊV LЕФУмБеШнЦїжаГфШы1 mol AКЭ1 mol BЃЌБЃГжКуЮТКубЙЯТЗДгІЃК
A(g)+B(g) C(g)ЃЛІЄH=ЃQ (QЃО0)
C(g)ЃЛІЄH=ЃQ (QЃО0)
ДяЕНЦНКтЪБЃЌCЕФЬхЛ§ЗжЪ§ЮЊ40%ЁЃЪдЛиД№гаЙиЮЪЬтЃК
(1)Щ§ЮТЪБЃЌCЕФЗДгІЫйТЪ________(ЬюЁАМгПьЁБЁАМѕТ§ЁБЛђЁАВЛБфЁБ)ЁЃ
(2)ШєЦНКтЪБЃЌБЃГжШнЦїШнЛ§ВЛБфЃЌЪЙШнЦїФкбЙЧПдіДѓЃЌдђЦНКт________ЁЃ
AЃЎвЛЖЈЯђе§ЗДгІЗНЯђвЦЖЏЁЁЁЁЁЁЁЁ ЁЁЁЁ BЃЎвЛЖЈЯђФцЗДгІЗНЯђвЦЖЏ
CЃЎвЛЖЈВЛвЦЖЏЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎВЛвЛЖЈвЦЖЏ
(3)ШєЪЙЮТЖШЁЂбЙЧПдкЩЯЪіЬѕМўЯТКуЖЈВЛБфЃЌдкУмБеШнЦїжаГфШы2
mol AКЭ2 mol B,дђЗДгІДяЕНЦНКт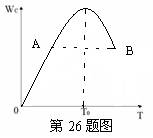 ЪБЃЌCЕФЬхЛ§ЗжЪ§ЮЊ________ЃЛШнЦїЕФШнЛ§ЮЊ________ЁЃ
ЪБЃЌCЕФЬхЛ§ЗжЪ§ЮЊ________ЃЛШнЦїЕФШнЛ§ЮЊ________ЁЃ
15ЃЎдкЯТСаЪТЪЕжаЃЌЪВУДвђЫигАЯьСЫЛЏбЇЗДгІЫйТЪЃК
(1)МЏЦјЦПжаH2КЭCl2ЕФЛьКЯЦјЬхЃЌдкЦПЭтЕуШМУОЬѕЪБЗЂЩњБЌеЈЃК_____________________ЁЃ
(2)ШлЛЏЕФKClO3ЗХГіЦјХнКмТ§ЃЌШіШыЩйСПMnO2КмПьВњЩњЦјЬхЃК_____________________ЁЃ
(3)ЭЌХЈЖШЁЂЭЌЬхЛ§ЕФбЮЫсжаЗжБ№ЗХШыЭЌбљДѓаЁЕФаПСЃКЭУОЬѕЃЌВњЩњЦјЬхгаПьгаТ§ЃК______________________________ЁЃ
(4)ЯФЬьЕФЪГЦЗвзУЙБфЃЌЖјЖЌЬьВЛвзЗЂЩњИУЯжЯѓЃК________________________ЁЃ
14ЃЎ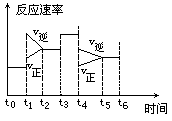 вЛУмЗтЬхЯЕжаЗЂЩњЯТСаЗДгІЃКN2 +3H2
вЛУмЗтЬхЯЕжаЗЂЩњЯТСаЗДгІЃКN2 +3H2  ЁЁ2NH3ЁЁЁЁ ІЄHЃМ 0ЃЌЯТЭМЪЧФГвЛЪБМфЖЮжаЗДгІЫйТЪгыЗДгІНјГЬЕФЧњЯпЙиЯЕЭМЃК
ЁЁ2NH3ЁЁЁЁ ІЄHЃМ 0ЃЌЯТЭМЪЧФГвЛЪБМфЖЮжаЗДгІЫйТЪгыЗДгІНјГЬЕФЧњЯпЙиЯЕЭМЃК
ЛиД№ЯТСаЮЪЬтЃК
(1)ДІгкЦНКтзДЬЌЕФЪБМфЖЮЪЧ______ЃЎ
(2)t1ЁЂt3ЁЂt4ЪБПЬЬхЯЕжаЗжБ№ЪЧЪВУДЬѕМўЗЂЩњСЫБфЛЏЃП
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)ЯТСаИїЪБМфЖЮЪБЃЌАБЕФАйЗжКЌСПзюИпЕФЪЧ______ЃЎ
AЃЎt0-t1ЁЁЁЁ BЃЎt2-t3ЁЁЁЁ CЃЎt3-t4ЁЁЁЁ DЃЎt5-t6
13ЃЎдкЯЁАБЫЎжаДцдкЦНКтЃКNH3+H2O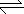 NH
NH +OHЃ,ШчНјааЯТСаВйзїЃЌдђNH3ЁЂNH
+OHЃ,ШчНјааЯТСаВйзїЃЌдђNH3ЁЂNH ЁЂH+ЁЂOHЃХЈЖШШчКЮБфЛЏЃПЪдгУЁАдіДѓЁБЁАМѕаЁЁБЁАВЛБфЁБЬюаДЁЃЁЁ
ЁЂH+ЁЂOHЃХЈЖШШчКЮБфЛЏЃПЪдгУЁАдіДѓЁБЁАМѕаЁЁБЁАВЛБфЁБЬюаДЁЃЁЁ
(1)ЭЈЪЪСПHClЦјЬхЪБЃЌc(NH3)ЁЁЁЁЁЁЁЁЁЁЁЁ ,c(H+)ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)МгШыЩйСПNaOHЙЬЬхЪБЃЌc(NH )ЁЁЁЁЁЁЁЁЁЁЁЁ
,c(OHЃ)ЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃЁЁ
)ЁЁЁЁЁЁЁЁЁЁЁЁ
,c(OHЃ)ЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃЁЁ
(3)МгШыNH4ClОЇЬхЪБЃЌc(NH )ЁЁЁЁЁЁЁЁЁЁЁЁ
,c(OHЃ)ЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃЁЁ
)ЁЁЁЁЁЁЁЁЁЁЁЁ
,c(OHЃ)ЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃЁЁ
12ЃЎНЋ0ЃЎ1molЁЄLЃ1CH3COOHШмвКМгЫЎЯЁЪЭЛђМгШыЩйСПCH3COONaОЇЬхЪБЃЌЖМЛсв§Ц№
AЃЎШмвКЕФpHдіМгЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁBЃЎДйНјCH3COOHЕФЕчРы
CЃЎШмвКЕФЕМЕчФмСІМѕШѕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎШмвКжаc(OHЃ)МѕЩй
11ЃЎЯТСаа№ЪіжаЃЌВЛФмгУЦНКтвЦЖЏдРэНтЪЭЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
AЃЎКьзиЩЋЕФNO2ЃЌМгбЙКѓбеЩЋЯШБфЩюКѓБфЧГ
BЃЎИпбЙБШГЃбЙгаРћгкКЯГЩSO3ЕФЗДгІ
CЃЎгЩH2ЁЂI2(g)ЁЂHI(g)ЦјЬхзщГЩЕФЦНКтЬхЯЕМгбЙКѓбеЩЋБфЩю
DЃЎЛЦТЬЩЋЕФТШЫЎЙтееКѓбеЩЋБфЧГ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com