
题目列表(包括答案和解析)
7、利用红外光谱对有机化合物分子进行测试并记录,可初步判断该有机物分子拥有的( )
A.同分异构体数B.原子个数 C.基团种类 D.共价键种类
6、在丙氨酸分子中,与手性碳原子直接相连的基团是 ( )
A.乙基 B.羟基 C.氨基 D醛基
5、目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确的是 ( )
A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B.碳原子性质活泼,可以跟多数元素原子形成共价键
C.碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键
D.多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合
4、下列关于常见有机物的说法不正确的是
A. 乙烯和苯都能与溴水反应 B. 乙酸和油脂都能与氢氧化钠溶液反应
C. 糖类和蛋白质都是人体重要的营养物质 D. 乙烯和甲烷可用酸性高锰酸钾溶液鉴别
3、2007年8月16日科技网报道,美国研究人员发现,艾滋病病毒通过两种方式伤害人脑,一种是杀死脑细胞,另一种是阻止新细胞的生成。感染艾滋病是艾滋病病毒首先通过人体gpl20蛋白质而引起病变,因此问题的关键对gpl20这种蛋白质的研究,下列推断正确的是 ( )
A.该病毒在盐溶液中一定发生变性
B.艾滋病病毒与gpl20在一定条件下水解最终都能产生氨基酸
C.温度越高,gpl20蛋白质活性越高
D.通常把艾滋病病毒样本保存在福尔马林中
2、居室空气污染的主要来源之一是人们使用的装饰材料、胶体板、内墙涂料释放出的一种刺激性气味的气体,该气体是 ( )
A.CH4 B.NH3 C.HCHO D.SO2
1、生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是 ( )
①人的皮肤在强紫外线的照射下将会失去生理活性 ②用甲醛溶液浸泡海产品保鲜
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④棉花和木材的主要成分都是纤维素,蚕丝和蜘蛛丝的主要成分都是蛋白质
⑤蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
A.①④⑤ B.②③④ C.①②④⑤ D.全部
31.工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为 。
(2)接触室内发生的反应为:
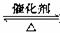 SO2(g)+
SO2(g)+
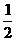 O2(g) SO3(g) △H=
a kJ•mol-1
O2(g) SO3(g) △H=
a kJ•mol-1
下表为不同温度(T)下该反应的化学平衡常数(K):
|
T/K |
673 |
723 |
823 |
923 |
|
K |
423 |
37.4 |
20.5 |
4.68 |
① 根据上表数据及化学平衡理论,上述反应中a 0(填“>”或“<”)。
② K值越大,表明反应达到平衡时 (填标号)。
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等。下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是 (填标号)。

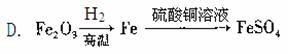
(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4•2H2O)。求:22.4 m3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0% )
30. 一定温度下,向如图所示带有可移动活塞的密闭容器中充入2 L
SO2 和1 L O2 的混合气体,发生如下反应2 SO2 (g) + O2 (g)  2
SO3 (g) 。
2
SO3 (g) 。
(1)若活塞可自由移动,平衡后,活塞停止在“2.1”处,则该反应中SO2 的转化率为____ ____。
(2)若开始时,充入容器的起始物质分别是
 ①2 L SO2
和1 L O2 ;
①2 L SO2
和1 L O2 ;
②2 L SO3 (g) 和 1 L N2 ;
③1 L SO2 、1 L O2 和 1 L SO3 (g),
使活塞固定在“3”处,达到平衡后,容器中SO3 (g)的体积分数大小关系是 (用序号和“<”、“=”、“>”表示)。
(3)向(1)平衡后的容器中充入0.2 mol 的SO3,活塞移动后再次达到平衡时,测得此过程中从外界共吸收了1.96 kJ 的热量。
写出SO2 发生氧化反应的热化学方程式:________ 。
29. Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com