
题目列表(包括答案和解析)
4.下列事实不能用勒沙特列原理解释的是 ( )
(A) 开启啤酒瓶后,瓶中马上泛起大量泡沫
(B) 钢铁在潮湿的空气中容易生锈
(C) 实验室中常用排饱和食盐水的方法收集氯气
(D) 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
3.下列物质转化需要加入还原剂才能实现的是( )
(A) SO32-→SO2 (B) HCl→Cl2 (C) Na→Na+ (D) SO2→S
2.下列离子在溶液中因发生氧化还原反应而不能大量共存的是 ( )
(A) H+、NO3-、Fe2+、Na+ (B) Ag+、NO3-、Cl-、K+
(C) K+、Ba2+、OH-、SO42- (D) Cu2+、NH4+、Br-、OH-
1.化学平衡研究的对象是 ( )
(A) 复分解反应 (B) 氧化还原反应
(C) 可逆反应 (D) 化合反应
28. (7分)碳酸钠晶体在加热时会失去全部结晶水,而碳酸钠本身不分解。
(7分)碳酸钠晶体在加热时会失去全部结晶水,而碳酸钠本身不分解。
Na2CO3·xH2O Na2CO3 +x H2O
现有一种碳酸钠晶体(Na2CO3·xH2O),为了测定其组成,某学生在不同温度下给试样加热(温度逐次升高),实验结果记录如下:
坩埚质量32.500g;(坩埚+晶体试样)的质量55.700g。
|
实验次数 |
温度(℃) |
冷却后(坩埚+试样)的质量(g) |
|
1 |
T1 |
48.500 |
|
2 |
T2 |
44.900 |
|
3 |
T3 |
43.100 |
|
4 |
T4 |
43.100 |
(1)第一次实验后,坩埚里剩余试样的质量是 g,试样晶体失去结晶水的质量是 g;
(2)第二次实验后,坩埚里剩余试样中含结晶水的百分含量为 (保留一位小数);
(3)计算确定碳酸钠晶体(Na2CO3 ·xH2O )中的x值。(第3小题要求写出计算过程)
(8)稀释原醋所用的蒸馏水为什么要先煮沸驱赶CO2?
___________________________________________________________
(9)原醋的总酸度是________g/100mL。
(10)中和滴定过程中,当其它操作均正确时,下列操作不会引起实验误差的是_________(填编号)
(a)滴定管水洗后直接装入标准液
(b)滴定过程中用洗瓶洗涤了锥形瓶内壁两次
(c)锥形瓶用蒸馏水洗净后,直接放入待测液进行测定
|
滴定次数 实验数据 |
1 |
2 |
3 |
4 |
|
V(待测液)/mL |
20.00 |
20.00 |
20.00 |
20.00 |
|
V(NaOH)/mL(初读数) |
0.00 |
0.200 |
0.10 |
0.00 |
|
V(NaOH)/mL(终读数) |
14.95 |
15.20 |
15.15 |
16.95 |
|
V(NaOH)/mL(消耗) |
14.95 |
15.00 |
15.05 |
16.95 |
(5)四次实验中明显误差的一组是_____________(填编号)。
(6)消耗NaOH溶液的平均值是_____________mL。
(7)待测液的浓度是_______________mol/L。
准确量取10.00mL原醋,配制成100.00mL待测食醋溶液(下称“待测液”)。完成该步骤,需要的一种定量仪器是__________(填仪器名称)
(2)量取一定体积的待测液
用红色手柄滴定管取20.00mL待测液于锥形瓶中。加1-2滴____________做指示剂
(3)盛装标准NaOH溶液,记录为NaOH标准溶液体积的初读数。
(4)滴定操作:滴定时一手控制___________,一手摇动_____________,眼睛注视___________________________直到滴定终点。判断滴定终点的现象是_________________________________________。记录NaOH的终读数。重复滴定4次。
27.(13分)食醋总酸量的测定
某实验小组拟用酸碱中和滴定法测定食醋的总酸量(CH3COOH,g/100mL)。
26.(6分)实验设计:
课题:用气体摩尔体积测定装置(如图所示)测定某铝合金样品中铝的质量分数(杂质不参与反应)。
提供试剂:铝合金样品、2mol/L的硫酸溶液、水。
(1)测定的原理是将样品与酸反应,生成的气体体积用下图装置进行测量。铝与酸反应的离子方程式是_________________________________。

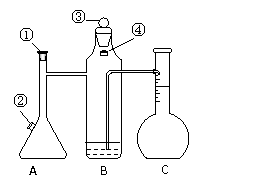

(2)实验的第一步操作是检查装置的气密性(②④都已塞严,①③的塞子未塞上,B中已加入一定量水,如图),下列操作和对应现象正确并能说明装置气密性良好的是________________(填编号)。
(a)先塞③,再塞①,此时观察到导管内液面上升
(b)塞③,从①处向A中加水,观察到导管内液面上升
(c)塞①③,用针筒从②插入,抽气,观察到B中导管有气泡
(d)塞①③, 手捂C,观察到B中导管有气泡
(3)为保证测定结果的准确性,仪器A中应预先盛放一定量的水,其目的一是稀释硫酸,降低反应速率,另一个目的是_____________________;实验过程中要三次使用注射器,则第二次使用注射器的操作是________
(填操作步骤)。
(4)准确称取0.107g样品,实验时加入酸的体积是8.0mL,仪器C的读数是128.8mL,抽气时注射器的读数是2.8mL,实验条件下的气体摩尔体积为23.65L/mol,则该样品中铝的质量分数是_______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com