
题目列表(包括答案和解析)
30、某化学兴趣小组要完成中和热的测定。
⑴实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1 盐酸、0.55mol·L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
⑵在大小烧杯之间填满碎泡沫塑料,其作用是__________________________________。实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
⑶他们记录的实验数据如下:
|
序 |
实 验 用
品 |
溶液温度 |
中和热 △H[ |
||
|
t1 |
t2 |
||||
|
Ⅰ |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.3℃ |
|
|
Ⅱ |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.5℃ |
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
计算上表中△H=
⑷若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响;缓慢逐滴加入盐酸,对测定结果 (填“有”或“无”)影响。
29、(8分)判断下过程的△H、△S大于零还是小零,用“>0”或“<0”填写下列表格
|
变化过程 |
△H |
△S |
|
NH4NO3溶于水 |
|
|
|
干冰(CO2)的升华 |
|
|
|
4Fe(s) + 3O2(g) =
2Fe2O3(s) |
|
|
|
CaCO3(s)分解为CaO(s)和CO2(g) |
|
|
28、(4分)已知:CO、H2、CH4的燃烧热分别为283 kJ/mol、286 kJ/mol、890 kJ/mol。
⑴ 写出表示氢气燃烧热的热化学方程式 。
⑵ 若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的取值范围是 。
27、(10分)某有机物A的结构简式为:(如下图)
⑴某同学对其可能具有的化学性质进行了如下预测,其中错误的是 。(填序号)
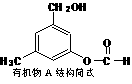 ①可以使酸性高锰酸钾溶液褪色;
①可以使酸性高锰酸钾溶液褪色;
②可以和NaOH溶液反应;
③在一定条件下可以和乙酸发生反应;
④在一定条件下可以发生消去反应;
 ⑤在一定条件下可以和新制Cu(OH)2反应;
⑤在一定条件下可以和新制Cu(OH)2反应;
⑥遇FeCl3溶液可以发生显色反应。
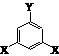
⑵该有机物的同分异构体甚多,其中有一类可以用 通式表示(其中X、Y均不为氢),试写出其中符合上述通式且能发生银镜反应的四种物质的结构简式:
, , , 。
26、(10分)某饱和一元醇的结构简式如右:则
⑴用系统命名法来命名该醇为:
⑵该醇的H-NMR谱中有______个峰,峰的面积比为___________;
⑶该醇在浓硫酸作用下发生消去反应,写出可能的有机产物的结构简式
25、对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);ΔH<0 的化学反应下列叙述不正确的是( )
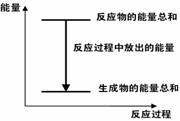 A.反应过程中能量关系可用右图表示
A.反应过程中能量关系可用右图表示
B.ΔH的值与反应方程式的计量系数有关[
C.若将该反应设计成原电池锌为负极
D.若将其设计为原电池当有32.5g锌溶解时,
正极放出气体一定为11.2L
试卷Ⅱ(非选择题,共50分)
24、近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为:KI+3H2O
 KIO3+3H2↑。下列有关说法中,正确的是 ( )
KIO3+3H2↑。下列有关说法中,正确的是 ( )
A.电解时,石墨做阳极,铁作阴极
B.电解时,在阳极上产生氢气
C.电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D.电解中,每转移0.5mol电子,理论上可得到0.1mol无水KIO3晶体
23、在2L的密闭容器中进行下列反应:A(g)+2B(g) 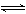 2C(g)+D(g)在一定条件下反应建立平衡,若条件不变,按下列各组物质加入起始物质,再次达到平衡后可能维持c(A)=c(B)=c(C)=0.2mol/L的一组是 ( )
2C(g)+D(g)在一定条件下反应建立平衡,若条件不变,按下列各组物质加入起始物质,再次达到平衡后可能维持c(A)=c(B)=c(C)=0.2mol/L的一组是 ( )
A.1mol A+2mol B+1mol C B.0.6mol C+0.6mol D+0.2mol B+0.3mol A
C.0.6mol A+0.2mol D+0.1mol C D.0.25mol A+0.5mol B+0.1mol C
22、一定条件下反应mA(g)+ nB(g) 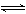 pC(g)+ qD(s)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( )
pC(g)+ qD(s)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( )
A.2、6、3、5 B.1、1、2、1 C.3、1、2、2 D.1、3、2、2
21、可逆反应:2A(g) + 3B(g) 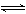 3C(g),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是 ( )
3C(g),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是 ( )
A.各物质的浓度之比为c(A)∶c(B)∶c(C) = 2∶3∶3
B.气体的总体积是反应开始时的 3/5
C.混合气体的密度不变
D.单位时间内, 若消耗了 a mol A 物质, 同时也消耗了 1.5 a mol 的C物质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com