
题目列表(包括答案和解析)
7.根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是 ( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2 溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4 溶液中加入浓盐酸,振荡后紫色褪去,产生黄绿色气体。
A.I2>Cl2>Fe3+>MnO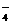 B.MnO
B.MnO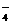 >Cl2>Fe3+>I2
>Cl2>Fe3+>I2
C.Cl2>I2>Fe3+>MnO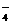 D.Fe3+>MnO
D.Fe3+>MnO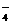 >Cl2>I2
>Cl2>I2
6.在5KCl+KClO3+3H2SO4→3Cl2↑+3K2SO4+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为 ( )
A.1∶1 B.5∶1
C.1∶5 D.3∶1
5.在3Cl2+6KOH→5KCl+KClO3+3H2O反应中,还原产物是·········· ( )
A.KClO3 B.KCl
C.KCl+H2O D.H2O
4.下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是···· ( )

 A.CO2+H2O H2CO3
B.Cl2+H2O HCl+HClO
A.CO2+H2O H2CO3
B.Cl2+H2O HCl+HClO
C.3Fe+4H2O(g) →Fe2O4+4H2 D.2Na+2H2O→2NaOH+H2↑
3.某元素在化学反应中由化合态变为游离态,则该元素·········· ( )
A.一定被氧化 B.一定被还原
C.既可能被氧化又可能被还原 D.以上都不是
2.下列化学反应基本类型中一定是氧化还原反应的是··········· ( )
A.化合反应 B.分解反应
C.复分解反应 D.置换反应
1.有关氧化还原反应的叙述正确的是·················· ( )
A.氧化还原反应的实质是有氧元素的得失
B.氧化还原反应的实质是元素化合价的升降
C.氧化还原反应的实质是电子的转移(得失或偏移)
D.物质所含元素化合价升高的反应是还原反应
30.将一定质量的镁铝合金溶解于100 mL某浓度的盐酸中(设体积变化忽略不计),在所得溶液中逐滴加入5mol/L的NaOH溶液,滴加过程中产生的沉淀的质量(y轴,单位是g),与所消耗的NaOH溶液的体积(x轴,单位为mL)的关系如下图所示。
求:
(1)合金中镁和铝的质量。
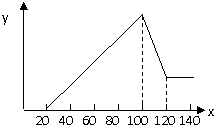
(2)所用盐酸的物质的量浓度。
29.某同学做探究同周期元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验方案和现象,如下表:
请你帮助该同学整理并完成实验报告。
(1)实验目的:____________________________________________________。
(2)实验用品:
仪器:试管、烧杯、砂纸、镊子、胶头滴管、滤纸、小刀、剪刀、__________。
药品:钠、镁条、铝片、新制H2S饱和溶液、新制氯水、2 mol/L盐酸、NaOH溶液、AlCl3溶液、蒸馏水、______________。
(3)实验内容:
|
实验方案 |
实验现象 |
|
①钠与滴有酚酞试液的冷水反应。 |
①钠块浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红。 |
|
②用砂纸擦后的镁带与沸水反应,再向反应液中滴加酚酞试液。 |
②产生少量气体,气体可燃,溶液变浅红色。 |
|
③镁带与2 mol/L的盐酸反应。 |
③反应十分强烈,产生可燃气体。 |
|
④铝条与2 mol/L的盐酸反应。 |
④反应,产生可燃气体。 |
|
⑤向AlCl3溶液中滴加NaOH溶液至过量。 |
⑤先有白色絮状沉淀,然后沉淀消失。 |
|
⑥向新制的H2S饱和溶液中滴加少量新制的氯水。 |
⑥_________________________。 |
产生实验现象⑥的离子方程式是_____________________________________,实验现象说明了Cl2和S相比,比较活泼的非金属是__________(填化学符号)
(4)实验结论:Na、Mg、Al元素的金属性随着原子序数的递增逐渐_____________(填“增强”、“减弱”或“不变”),S、Cl元素的非金属性随着原子序数的递增逐渐________________(填“增强”、“减弱”或“不变”)。
(5)问题与讨论:请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质对比情况。_________________________________________________________
______________________________________________________________。
28.铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水,但能溶于人体中的胃酸(主要是盐酸)。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

试回答下列问题:
(1)试剂1是__________________(填化学式),溶解后,静置后溶液略带淡黄色,说明溶液中已有了_______________(填离子符号)离子。酸性条件下,空气中静置,发生反应生成该离子的离子方程式是____________________________________。
(2)试剂2可以是__________________(填化学式)。加入新制氯水后发生反应的离子方程式是______________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com