
题目列表(包括答案和解析)
5.下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O
 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.对CO(g) + NO2 (g)  CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深
CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深
C.升高温度能够增大硝酸钾在水中的溶解度
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
4.把足量铝条放入盛有一定体积的稀盐酸的试管中,可使反应速率降低且不影响H2产生量的操作是
A.加入适量FeCl3溶液 B.加入适量KNO3溶液
C.加入适量的K2CO3溶液 D.加入适量Na2SO4溶液
3.四位同学同时进行反应:A(g)+3B(g)=2C(g)+2D(g) 的速率测定实验,分别测得反应速率如下:① v(A)= 0.15mol/(L·s)②v(B)= 0.6mol/(L·s) ③v(C)= 0.4mol/(L·s)④v(D)= 0.45mol/(L·s)。其中,反应进行得最快的是
A.① B.② C.③ D.④
2.下列说法不正确的是
A、焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行
B、自发进行的反应一定能迅速进行
C、在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大
D、一个反应能否自发进行,与焓变和熵变的共同影响有关
1.下列对化学反应的认识错误的是
A.会引起化学键的变化 B.会产生新的物质
C.必然引起物质状态的变化 D.必然伴随着能量的变化
31.(9分)常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1︰2的体积比混合,所得溶液的pH=12。用上述NaOH溶液滴定pH=3的某一元弱酸溶液20ml,达到终点时消耗NaOH溶液13ml,试求:
(1)NaOH溶液的物质的量浓度
(2)此一元弱酸的物质的量浓度
(3)求此条件下该一元弱酸的电离平衡常数
30.(4分)用标准的NaOH溶液滴定未知浓度的盐酸(盛于锥形瓶中),造成测定结果偏高的原因可能是 。
A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.未用标准液润洗碱式滴定管
29.(15分)用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品,所用的仪器是 、 、 。
(2)将样品配成250mL待测液,还需的仪器有 、 、 。
(3)取10.00mL待测液,用 量取。
(4)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,选用酚酞为指示剂,滴定时 手旋转酸式滴定管的玻璃活塞, 手不停地摇动锥形瓶,两眼注视 ,直到滴入一滴标准盐酸时溶液立即由 色变成 色,且 ,则达到滴定终点。
(5)根据下列数据,计算待测烧碱溶液的物质的量浓度: 。
|
滴定次数 |
待测液体积 (mL) |
标准盐酸体积(mL) |
|
|
滴定前读数(mL) |
滴定后读数(mL) |
||
|
第一次 |
10.00 |
0.50 |
20.40 |
|
第二次 |
10.00 |
4.00 |
24.10 |
28.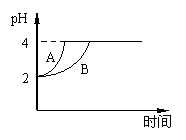 (4分)常温下,取pH=2的盐酸和醋酸溶液各100mL,
(4分)常温下,取pH=2的盐酸和醋酸溶液各100mL,
向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化
如右图所示。则图中表示醋酸溶液中pH变化曲线的是
(填“A”或“B”)。设盐酸中加入的Zn质量为m1, 醋酸溶液
中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)
27.(5分)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。则该溶液呈 性。在分析该溶液遇酚酞呈红色原因时,甲同学认为盐溶液应呈中性,所以可能是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com