
题目列表(包括答案和解析)
4. CaCl2的水溶液呈中性,HClO的水溶液呈酸性。
[交流讨论]该小组同学经过分析得出:HClO分解时除生成HCl外,生成的另一种常见气体是 。
[实验探究]
|
实验步骤 |
实验现象 |
实验结论 |
|
把少量漂白粉样品加入水中,通入足量的CO2气体,
。 |
。 |
漂白粉的漂白作用已失效。 |
[继续探究]同学们对失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对失效后的漂白粉成分进行猜想:
猜想一:CaCl2和CaCO3;
猜想二: ;
小明同学认为猜想中的成分CaCO3,除漂白粉的有效成分在空气中发生反应生成外,还有其它来源,请你用化学方程式表示 。
小聪同学进行实验证明猜想一成立,小聪同学的实验方案: 。
3. HClO不稳定,易分解生成HCl和一种常见的无色无味气体。
2.Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应
Ca(ClO)2+H 2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液 褪色。
2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液 褪色。
1.漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是 Ca(ClO)2。
33. (7分)某化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。
(7分)某化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。
[查阅资料]
31.(6分)根据下图回答问题。

请回答以下问题:
(1)装置中标“a”的仪器名称是_____。
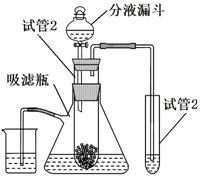 (2) 实验室加热高锰酸钾制取氧气的化学方程式为
,反应的发生装置为_______
(填序号,下同),收集装置是C或_______,选用这两种收集方法的原因是__________;若选用B装置制取氧气,反应的化学方程式为_________。
(2) 实验室加热高锰酸钾制取氧气的化学方程式为
,反应的发生装置为_______
(填序号,下同),收集装置是C或_______,选用这两种收集方法的原因是__________;若选用B装置制取氧气,反应的化学方程式为_________。
32.(6分)某化学研究性学习小组的同学们做了三个趣味实验,装置如右图(气密性良好)。当开启分液漏斗的旋塞,液体滴入盛有固体的试管2中时,观察到不同的现象。
(1)若试管2中发生了化学反应,观察到试管1中有气泡产生,且其中的石蕊溶液变红,试管2中发生反应的化学方程式为 。
(2)若试管2中没有发生化学反应,观察到两支导管口同时冒
气泡、吸滤瓶内的石灰水变浑浊,则试管2中的固体可能是____________。
(3)若观察到吸滤瓶内盛有的红色溶液变无色,分液漏斗中的液体、试管2中的固体分别是____________;烧杯中的液体可能是__________。请你解释溶液变色的原因:_______________。
30.(7分)甲、乙、丙为初中化学常见物质,甲分别能与乙和丙发生反应,乙又能与其它 物质发生反应得到丙。回答下列问题:
物质发生反应得到丙。回答下列问题:
(1)若甲、丙分别是气体单质,乙是固体单质。
①甲的化学式是_____;② 乙转化为丙的化学方程式是 。
(2)若甲、乙是氧化物,丙可用于改良酸性土壤。
则甲、丙的化学式分别是 。
(3)若乙、丙类别(指单质、酸、碱、盐或氧化物)相同,且甲、乙、丙中均含有一种相同元素,
①乙转化为丙的化学方程式是 , ②反应的基本类型是 。
(4)若甲是一种酸。下列说法中,正确的是 (填序号)。
①乙、丙可能都是 单质 ②乙、丙可能都是盐
单质 ②乙、丙可能都是盐
③丙一定不能转化为乙 ④三个反应可能都是置换反应
29.(6分)金属在生产生活中应用广泛。
(1)每年因金属锈蚀造成很大浪费,铁生锈的条件是__________;废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为________________;
 (2)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液。他们想从
(2)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液。他们想从 中回收金属铜和硫酸亚铁晶体,设计了如下方案:
中回收金属铜和硫酸亚铁晶体,设计了如下方案:
①写出Ⅰ中有关反应的化学方程式 。
②小红、小强同学在步骤Ⅰ中X能否改用锌的问题上产生了分歧。请你也参与他们的讨论,表明观点,并说明理由 。
(3)某工厂为防止环境污染和回收金属,向含有AgNO3和Cu(NO3 )2的废液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,能得出的结论是
(填序号)。
)2的废液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,能得出的结论是
(填序号)。
A.滤渣中一定没有Fe B.滤渣中一定有Ag,可能有Cu
C.滤液中一定有Fe(NO3)2,一定没有AgNO3 D.滤液中一定有Fe(NO3)2和Cu(NO3)2
28.(6分)水是重要的自然资源,在生产、生活和科研中有重要意义。
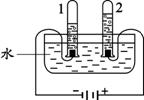 (1)右图是水的电解实验,反应的化学方程是为
。
(1)右图是水的电解实验,反应的化学方程是为
。
(2)医院使用的生理盐水是溶质质量分数为0.9%的 (填化学式)溶液。
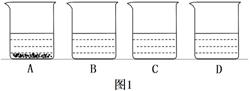
(3)水是一种最常用的溶剂。在A、B、C、D四个烧杯中分别装有等量的水,在t℃时,向A、B、C烧杯中分别加入25g、15g、5g甲物质,向D烧杯加入25g乙物质,充分溶解后,静置,现象如下图1所示。
回答下列问题:
①在图1四个烧杯的溶液中, (填“A”、“B”、“C”或“D”,下同)烧杯中的溶液一定是饱和溶液。
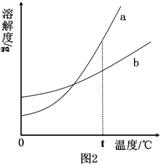
②图2分别为两种物质的溶解度曲线,其中可表示乙物质的是 (填“a”或“b”);要使A烧杯中剩余固体继续溶解,可采用的方法是 。
③室温下,将一瓶a溶液敞口放置一段时间,溶质质量分数由5%变了10%,放置前后溶液中所含水(溶剂)的质量比为 。
27.(6分)随着经济的发展,能源与环境成为人们日益关注的问题。
 (1)化石燃料包括煤、天然气和
。生活中若发生火灾时,常用的灭火材料有水、沙子、泡沫灭火器等。利用沙子灭火的主要原理是 。
(1)化石燃料包括煤、天然气和
。生活中若发生火灾时,常用的灭火材料有水、沙子、泡沫灭火器等。利用沙子灭火的主要原理是 。
(2)目前我区很多家庭仍在使用液化石油气作为燃料。
请回答:
①根据右图提供的信息归纳丁烷的化学性质有 ;
②写出丁烷在空气中燃烧生成二氧化碳和水的化学方
程式 。
(3)“低碳生活”是指减少能源消耗、节约资源,从而减少
二氧化碳排放的生活方式。下列做法中符合“低碳生活”
理念的是 。
A.大力发展火力发电 B.研制和开发新能源替代传统能源
C.分类处理生活垃圾 D.优化建筑设计,增强室内自然采光,减少照明用电
(4)当空气受SO2严重污染时,可通过飞机喷洒X粉末,使空气中的SO2含量明显降低,该过程发生的反应是2X +2SO2+O2==2CaSO4 +2CO2。X的化学式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com