
题目列表(包括答案和解析)
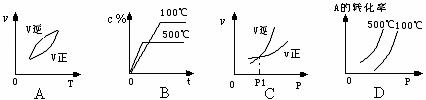
15.用来表示可逆反应2A(g)+B(g)  2C(g)(正反应是吸热反应)的正确图象是
2C(g)(正反应是吸热反应)的正确图象是
14.HClO是比H2CO3更弱的酸,反应:Cl2+H2O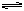 HCl+HClO达到平衡后,要使HClO浓度增加,可以加入:
HCl+HClO达到平衡后,要使HClO浓度增加,可以加入:
A、NaOH B、HCl C、CaCO3(固) D、H2O
13.一定温度下,将a mol PCl5通入一个容积固定不变的密闭容器中,发生反应:
PCl5(g)  PCl3(g)+Cl2(g),反应达到平衡时,测得混合气体的压强为p1,此时再向容器中通入a mol PCl5,同样温度下再达到平衡时,测得压强为p2,下列判断正确的是
PCl3(g)+Cl2(g),反应达到平衡时,测得混合气体的压强为p1,此时再向容器中通入a mol PCl5,同样温度下再达到平衡时,测得压强为p2,下列判断正确的是
A、2p1>p2 B、PCl5的分解率增大
C、p1>p2 D、Cl2的体积分数增大
12.对于相同物质的量浓度、相同体积的盐酸和醋酸,下列几种说法正确的是
A、它们起始时溶液中的c(H+)不相同
B、各用水稀释一倍后,pH比较:盐酸>醋酸
C、分别和同浓度的氢氧化钠溶液反应至pH=7,所用氢氧化钠溶液的体积相同
D、各与足量的锌粒充分反应,产生H2的量不同
11、用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
(A)白醋中滴入石蕊试液呈红色
(B)同样的锌粒分别和pH相等的白醋和盐酸反应,开始时速率相等。
(C)蛋壳浸泡在白醋中有气体放出
(D)pH试纸显示醋酸的pH为2-3
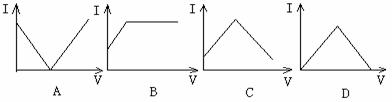
10.向某氨水中加入醋酸溶液,其导电能力(I)与加入醋酸溶液的体积(V)关系正确的是(见图)
9.实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
A、K2SO4固体 B、NaOH溶液 C、(NH4)2SO4粉末 D、CH3COONa固体
8.把0.6mol X气体和0.4mol Y气体混合于2L容器中,发生如下反应:
3 X (g)+Y (g)  n Z (g)+2 W (g),5min末已生成0.2mol W,若测知以Z浓度变化来表示的平均速率为0.01mol/(L·min)。上述反应中Z气体的化学计量数n的值是
n Z (g)+2 W (g),5min末已生成0.2mol W,若测知以Z浓度变化来表示的平均速率为0.01mol/(L·min)。上述反应中Z气体的化学计量数n的值是
A、1 B、2 C、3 D、4
7.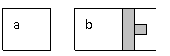 如右图所示:等温时,a、b容器开始体积相等,各充入等量的SO3(g),则平衡时SO3的
如右图所示:等温时,a、b容器开始体积相等,各充入等量的SO3(g),则平衡时SO3的
转化率大小关系是
(A) a>b (B) a<b
(C) a=b (D) 无法确定
6.废气中的氮氧化合物是主要的大气污染源之一,为了保护环境,工业上常通入氨与之发生如下反应:NOx+NH3 ® N2+H2O,使之转化为无毒的N2。现有NO2和NO的混合气体3L,通入3L(同温、同压下)NH3恰好使其完全转化为N2。原混合气体中NO2和NO的物质的量之比为
A、1∶1 B、2∶1 C、3∶1 D、1∶4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com