
题目列表(包括答案和解析)
19、(8分)
(1)① > (2分) ②9.9×10-7(2分) 1.0×10-8 (2分) (2)NaA和NaOH(2分)
24、(8分)在温度为373K时,把11.5g N2O4气体通入体积为500ml的真空密闭容器中立即出现红棕色,反应进行到2s时,NO2含量为0.01mol,进行到60s时,达到平衡,此时容器中混合气体的密度是氢气密度的28.75倍,则:
(1)开始时2s内以c(N2O4)的变化表示的反应速率是 .
(2)达到平衡时体系内的压强是开始的________________倍
第I卷选择题 答案(共54分)
第II卷非选择题 答案(共46分)
23、(6分)在一个固定体积的,向容器中充入2molA和1molB,发生如下反应:
2A(g) + B(g)  3C(g) + D(s),反应达到平衡时C的浓度为1.2mol/L。
3C(g) + D(s),反应达到平衡时C的浓度为1.2mol/L。
(1)若使容器温度升高,平衡时混合气体的平均摩尔质量减小,则正反应为________(填“吸热”或“放热”)反应。
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是_________(用序号填空)
①4molA+2molB ②3molC+1molD+lmolB
③3molC+2molD ④1.6molA+0.8molB+0.3molC
(3)某温度下,若向容器中加入3molC和0.8mo1D,反应达到平衡时C的浓度仍为1.2 mol/L,则容器的容积V(L)的取值范围为 。
22、(10分)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol/L酸性KMnO4和未知浓度的无色NaHSO3溶液,反应的离子方程式是:2MnO4―+5HSO3―+H+=2Mn2++5SO42―+3H2O。填空回答问题:
(1)不用______(酸、碱)式滴定管盛放KMnO4溶液,原因是___ ______________。
(2)指示剂如何选择? ,说明理由_____________________________________。
(3)滴定前平视KMnO4液面,刻度为amL,滴定后俯视液面刻度为bmL,则(b-a)mL比实际消耗KMnO4溶液体积_____________(多、少)。根据(b-a)mL计算得到的待测液浓度,比实际浓度____________(大、小)。
21、(6分)已知25℃时0.1mol·L-1醋酸溶液的pH约为3。向其中加入少量醋酸钠晶体,待晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)、你认为上述两种解释中 (“甲”或“乙”)正确。
(2)、①为了验证上述哪种解释正确,继续做如下实验:向0.1mol·L-1的醋酸溶液中加入少量下列物质 (填写编号),然后测定溶液的pH。
A.固体CH3COOK B.固体CH3COONH4 C.气体NH3 D.固体NaHCO3
②按照你的判断,加入上述物质后,溶液pH应 (填“增大”或“减小”或“不变”)。(已知25℃时0.1mol·L-1氨水和0.1mol·L-1醋酸的电离程度相同)
20、 (8分)现有下列各坐标图:
(8分)现有下列各坐标图:
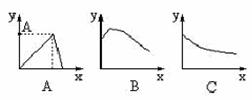
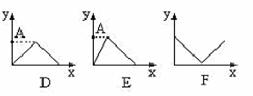
(1)x轴坐标代表加水量,y轴代表c(H+),能表示出0.1mol/L醋酸在稀释时的状况的坐标图是 。
(2) x轴代表在氢氧化钡溶液中滴加硫酸的量,y轴代表溶液导电性的变化,符合这一关系的坐标图是 。
(3) x轴代表向1L 0.01mol/L石灰水中通入CO2的质量(g),y轴代表沉淀质量(g)的变化,符合这一情况的坐标图是 ,A点的数值为 g。
19、(8分)(1)如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
①混合溶液中由水电离出的c(H+) 0.1mol/LNaOH溶液中由水电离出的c(H+)。(填“>”、“<”、或“=”)
②求出混合物中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)= mol/L c(OH-)-c(HA)= mol/L
(2)在含有A、Na+、H+、OH-的水溶液中,若其浓度大小关系为c(Na+)>c(OH-)>c(A-)>c(H+),则溶液中的溶质可能 。
18、在容积一定的密闭容器中,可逆反应A2(g)+ B2(g)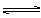 xC(g)
符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是
xC(g)
符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是

A.P3<P4,Y轴表示A2的转化率
B.P3<P4,Y轴表示A2的浓度
C.P3>P4,Y轴表示混合气体的密度
D.P3>P4,Y轴表示混合气体的平均摩尔质量
第II卷(非选择题 共46分)
17、室温时,将x mL pH=a 的稀NaOH溶液与y mL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是
A.若x=y,且a+b=14,则pH>7
B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7
D.若x=10y,且a+b=14,则pH>7
16、下列事实与盐类水解有关的是
①NaHCO3溶液呈碱性
②NaHSO4溶液呈酸性
③长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结
④加热能增加纯碱的去污能力
⑤配制CuCl2溶液,用稀盐酸溶解CuCl2固体
⑥明矾能净水
⑦氯化铵溶液可作焊药去除金属制品表面的锈斑
⑧加热FeCl3·6H2O晶体,往往得不到FeCl3固体
⑨NH4F溶液不能用玻璃瓶盛放。
A.全部 B.除②⑦以外 C.除②以外 D.除⑨以外
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com