
题目列表(包括答案和解析)
5、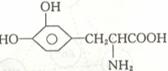 L-多巴是一种有机物,可用于帕金森综合症的治疗,其结构简式如下:下列关于L-多巴的叙述中不正确的是 ( )
L-多巴是一种有机物,可用于帕金森综合症的治疗,其结构简式如下:下列关于L-多巴的叙述中不正确的是 ( )
A.长期暴露在空气中易变质 B.既有酸性,又有碱性
C.一定条件下能发生聚合反应 D.分子中只有6个碳原子共平面
4、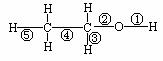 乙醇分子中不同的化学键如右图。下列关于乙醇在不同的反应中断裂化学键的说法
乙醇分子中不同的化学键如右图。下列关于乙醇在不同的反应中断裂化学键的说法
错误的是( )
A.与金属钠反应时,键①断裂 www.k&s5*
B.在Cu催化下与O2反应时,键①、③断裂C.与乙酸在浓硫酸作用下反应时,键②断裂
D.与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂
3、下列有机物命名正确的是 ( )
A. 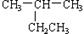 2-乙基丙烷 B. CH3CH2CH2CH2OH 1-丁醇
2-乙基丙烷 B. CH3CH2CH2CH2OH 1-丁醇
C. 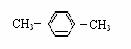 间二甲苯 D.
间二甲苯 D. 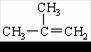 2-甲基-2-丙烯
2-甲基-2-丙烯
2、下列物质的类别与所含官能团都正确的是
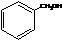
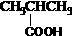 A.
酚类
-OH
B.
酯类 -COOH
A.
酚类
-OH
B.
酯类 -COOH
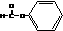
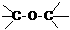
C. 醛类 –CHO D. CH3-O-CH3 醚类
1、目前车用乙醇汽油正逐步推广使用。它是把变性燃料乙醇和汽油按一定比例混配形成的一种新型汽车燃料。经多项检测结果表明,它不影响汽车的行驶性能,还可以减少有害气体的排放量。下列有关乙醇汽油的说法正确的是 ( )
A.乙醇汽油是一种纯净物
B.乙醇汽油作燃料不会产生碳氧化合物等有害气体,其优点可以减少对环境的污染
C.乙醇和汽油都可作溶剂,也可相互溶解 D.乙醇和乙二醇互为同系物
22、(10分)已知反应FeO(s)+CO(g) = Fe(s)+CO2(g) 的平衡常数K=0.5(1273K)。若起始浓度c(CO) = 0.05 mol·L-1,c(CO2) = 0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加的FeO量会不会促使平衡向正方向移动?
21、(8分) (1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应:____________________________________________________;
银片上发生的电极反应:_____________________________________________________。
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算产生氢气的体积(标准状况)。
20、(16分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的H表示生成l mol产物的数据)。
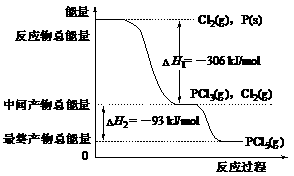
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是________________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式是________________________________________。上述分解反应是一个可逆反应。温度Tl时,在密闭容器中加入0.80 mol PCl5,反应达平衡时PCl5还剩0.60 mol,其分解率al等于_____________;若反应温度由Tl升高到T2,平衡时PCl5的分解率为a2,a2_________ al(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是__________________________________________________。
(4)P和Cl2分两步反应生成1 mol PCl5的H3 = ________________,一步反应生成1 mol PCl5的H4______H3(填“大于”、“小于”或“等于”)。
19.(9分)依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。
 请回答下列问题:
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是___________;
(2)银电极为电池的________极,
发生的电极反应为_____________________________________________;
X电极上发生的电极反应为_____________________________________;
(3)外电路中的电子是从_______电极流向________电极。
18.(6分)已知下列两个热化学方程式:
H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ·mol-1
C3H8(g)+5O2(g)= 3CO2(g)+4H2O(l) △H=-2220.0kJ·mol-1
(1)实验测得H2和C3 H8的混合气体共5 mol,完全燃烧生成液态水时放热6264.5kJ,则混合气体中H2和C3 H8的体积比是_______ ;
(2)已知:H2O(l)==H2O(g) △H=+44.0kJ·mol-1,写出丙烷燃烧生成CO2和气态水的热化学方程式__________________________________________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com