
题目列表(包括答案和解析)
8.25℃时,水的电离可达到平衡:H2O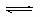 H++OH- △H>0,下列叙述正确的是( )
H++OH- △H>0,下列叙述正确的是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
 D. 将水加热,Kw增大,pH不变
D. 将水加热,Kw增大,pH不变
7.将 lmolSO2和 l mol O2 通入体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡时 SO3为0.3mol,若此时移走 0.5mol O2和 0.5mol SO2则反应达到新的平衡时,SO3的物质的量是( )
A.0.3mol B.0.15mol
C.小于 0.15mol D.大于0.15mol而小于 0.3mol
6.已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)  H2(g)+I2(g)的化学平衡常数为( )
H2(g)+I2(g)的化学平衡常数为( )
A、50 B、0.02 C、100 D、无法确定
5.一定条件下反应2AB(g) 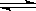 A2(g)+B2(g)达到平衡状态的标志是( )
A2(g)+B2(g)达到平衡状态的标志是( )
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内,3种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
4.已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的( )
2AB2(g)△H <0,下列说法正确的( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
3.用食用白醋(醋酸浓度约1 mol•L-1)进行下列实验,能证明醋酸为弱电解质的是( )
A. 白醋中滴入石蕊试液呈红色 B. 白醋加入豆浆中有沉淀产生
C. 蛋壳浸泡在白醋中有气体放出 D. pH试纸显示白醋的pH为2~3.
2. 下列物质容易导电的是( )
A. 氯化钠晶体 B. 无水乙醇 C. 硝酸钾溶液 D.蔗糖溶液
1.下列热化学方程式中的反应热又为燃烧热的是( )
A.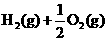 ══
══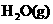
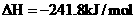
B.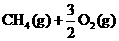 ══
══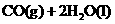

C.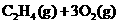 ══2CO2(g)+2H2O(l)
══2CO2(g)+2H2O(l)

D.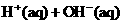 ══
══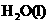
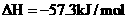
21.(7分)某一氯代烷3.70g跟足量的NaOH溶液混合加热后,用HNO3酸化,再加适量的
AgNO3溶液,生成5.74gAgCl白色沉淀。
(1)通过计算,写出这种一氯代物的分子式以及它的所有同分异构体的结构简式
(2)如果一氯代物和足量的NaOH溶液混合加热后,没有用HNO3加以酸化,就加入
AgNO3溶液,能否根据生成沉淀的质量来推断这种氯代烃的分子式?试加以说明。
20.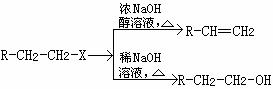 (10分)已知:(X代表卤素原子,R代表烃基)
(10分)已知:(X代表卤素原子,R代表烃基)
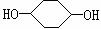
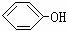 利用上述信息,按以下步骤从
合成
(部分试剂和反应条件
利用上述信息,按以下步骤从
合成
(部分试剂和反应条件
已略去)
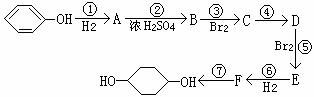 请回答下列问题:
请回答下列问题:
(1)分别写出 B、D的结构简式:
B 、D 。
(2)写出反应①、②、⑦的反应类型:① 、② 、⑦ 。
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为 。
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件)
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com