
题目列表(包括答案和解析)
21.(8分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合恰好完全反应,生成氮气和水蒸气,放出256 kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 ▲ 。
(2)又已知16g液态肼与液态双氧水反应生成液态水时放出的热量是408 kJ。
则H2O(l)=H2O(g) 的ΔH= ▲ kJ•mol-1。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 ▲ 。
20.对下列实验的描述正确的是( )
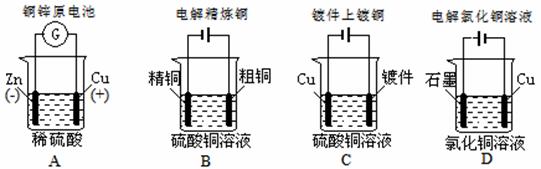
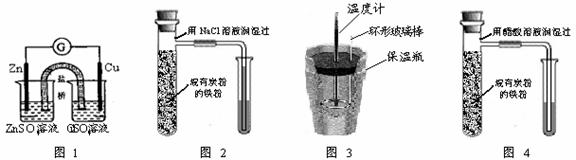 A.图1所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
A.图1所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
B.图2所示的实验:根据小试管中导管液面的变化判断铁粉发生了析氢腐蚀
C.图3所示的实验:根据温度计读数的变化用浓硫酸和NaOH反应测定中和热
D.图4所示的实验:根据小试管中导管液面的变化判断铁粉发生了吸氧腐蚀
19.市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li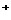 的高分子材料。这种锂离子电池的电池反应为:Li+2Li
的高分子材料。这种锂离子电池的电池反应为:Li+2Li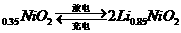 下列说法不正确的是( )
下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e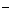 =Li
=Li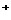
B.充电时,Li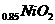 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li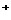 向负极移动
向负极移动
18.铅蓄电池的电极材料是Pb和PbO2,电解液是硫酸溶液。现用铅蓄电池电解饱和硫酸钠溶液
一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是( )
A.蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4
B.电解池的阳极反应式为:4OH-- 4e-==2H2O + O2↑
C.电解后,c(Na2SO4)不变,且溶液中有晶体析出
D.蓄电池中每转移2mol电子,电解池中就消耗1molH2O
17.用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A. ①② B.②③ C.②④ D.③④
16.下列图示中关于铜电极的连接错误的是( )
15.已知H2(g)、C2H4(g)和C2H5OH(1)的标准燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1 C.-330kJ·mol-1 D.+330kJ·mlo-1
14.已知:H2(g)+F2(g)==2HF(g) △H=-270 kJ/mol,下列说法正确的是( )
A.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
B.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
C.在相同条件下,2mol氟化氢气体的键能总和小于1mol氢气和1mol氟气键能之和[D.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
13.在同温同压下,下列各组热化学方程式中, △H1>△H2的是( )
A. 2H2(气)+O2(气)=2H2O(液) △H1 2H2(气)+O2(气)=2H2O(气) △H2
B. S(气)+O2(气)=SO2(气) △H1 S(固)+O2(气)=SO2(气) △H2
C.H2(气)+Cl2(气)=2HCl(气) △H1 1/2H2(气) +1/2Cl2(气)=HCl(气) △H2
D.C(固)+1/2O2 (气)=CO(气) △H1 C(固)+O2 (气)=CO2(气) △H2
12.已知299 K时,合成氨反应 N2 (g ) + 3H2 (
g ) 2NH3 ( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
2NH3 ( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
A.一定大于92.0 kJ B.一定等于92.0 kJ C.一定小于92.0 kJ D.不能确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com