
题目列表(包括答案和解析)
2、下列属于电离方程式且书写正确的是( )
A、H3O++OH-=H2O+H2O B、NaHCO3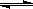 Na++H++CO32-
Na++H++CO32-
C、H2O+H2O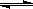 H3O++OH- D、H3PO4
H3O++OH- D、H3PO4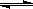 3H++PO43-
3H++PO43-
1、下列说法不正确的是( )
A、铁生锈、氢燃烧均为自发放热过程
B、冰融化过程其熵值增加
C、硝酸铵溶于水的过程ΔH>0,所以不是自发过程
D、同一物质固态时熵值最小
29.丙烯可用于合成杀除根瘤线虫的农药(分子式为C3H5Br2Cl)和应用广泛的DAP树脂;
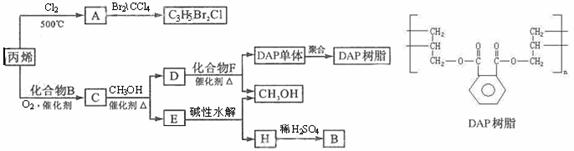 已知酯与醇可以发生如下酯交换反应:
已知酯与醇可以发生如下酯交换反应:
(I):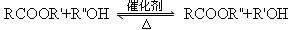 (R,R’ R’’代表羟基)
(R,R’ R’’代表羟基)
(Ⅱ):C与甲醇的反应和D与F的反应均属于酯交换反应。
(1)农药C3H5Br2Cl分子中每个碳原子上均连有卤原子。
①A的结构简式是______________________
A 含有的官能团名称是______________________;
②由丙烯生成A的反应类型是______________________
(2)A水解可得到D,该水解反应的化学方程式是______________________。
(3)C蒸汽密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为
碳60%,氢8%,氧32% ,C的结构简式是______________________。
(4)下列说法正确的是(选填序号字母)___________
a. C能发生聚合反应,还原反应和氧化反应
b. C含有两个甲基的羧酸类同分异构体有4个
c. D催化加氢的产物与B具有相同的相对分子质量
d. E有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环利用DAP树脂的制备。其中将甲醇与H分离的操作方法是______________________
(6)F的分子式为C10H10O4 ;DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式_________________________。
28.某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;
二是发生双水解反应: 2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,需要用到纯净的氯化铁和亚硫酸钠,同学们经过讨论设计并实施了下列实验,请填写下列空白:
[实验Ⅰ]学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,作者设计这个实验的目的是 ______________________。
[实验Ⅱ]取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是 ,向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是 ;将该溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生血红色现象的离子方程式是 。
[实验Ⅲ]换用稀释的FeCl3和Na2SO3溶液重复上述实验,实验Ⅲ产生的现象与实验Ⅱ完全相同。由上述实验得出的结论是 。
[实验Ⅳ]若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是_______________________________________________。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①___________________________________;②________________________________。
27. A、B、C、D、E、F、G都是元素周期表中前20号元素,原子序数依次增大。
①A、D同主族,C和F同主族;
②B分别与A、C、F形成的化合物分子均呈正四面体结构,且B位于正四面体的体心;
③D、E、F同周期,且D、E、F的最高价氧化物的水化物两两混合均能发生反应生成盐和水。
根据以上信息,回答下列问题:
(1)C和F氢化物中,沸点较低的是 (选填“C” 或“F”);
(2)B分别与A、C、F所形成的分子中沸点由高到低的顺序为: (填分子式用“>”隔开);
(3)C和D的离子中,半径较小的是 (填离子符号)。
(4)元素E与F形成的化合物沸点为182.7℃,易升华,它在熔融状态下不导电,但在水溶液中能够能够导电,属于强电解质,该固体化合物的晶体类型为: 。
(5)D、E的最高价氧化物的水化物发生反应生成盐和水的离子方程式: 。
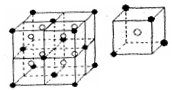 (6)C和G可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如右图所示,阳离子(用“●”表示)位于该正方体的顶点或面心;阴离子(用“〇”表示)均位于小正方体中心。
(6)C和G可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如右图所示,阳离子(用“●”表示)位于该正方体的顶点或面心;阴离子(用“〇”表示)均位于小正方体中心。
该化合物的电子式是 。
26.按要求填空。
①NaCl晶体:在NaCl晶体中,每个Na+周围与之最接近且等距离的Cl-有 个,这几个Cl-在空间的几何构型为 。
②SiO2晶体:在SiO2晶体中,每个Si原子周围结合 个O原子,同时每个O原子跟 个Si原子相结合。4.5g SiO2晶体中Si-O键的个数为 NA。
③CO2晶体:CO2和SiO2的晶体结构不同。在CO2晶体中,每个CO2分子周围有 个与之最近且等距离的CO2分子,距离为 。(设晶胞边长为a,用a表示)
④白磷晶体:白磷(P4)分子的空间结构为 ,31g白磷中P-P键的数目为 NA;
若将1分子白磷中的所有P-P键打开并各插入一个氧原子,则1分子白磷可结合 个氧原子。
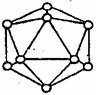 ⑤晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____个硼原子组成,共含有______B-B键。(背面图形无法画出)
⑤晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____个硼原子组成,共含有______B-B键。(背面图形无法画出)
⑥胶体的制备:将少量饱和的氯化铁溶液滴入沸水中,可制备氢氧化铁胶体。
离子反应方程式如下: 。
25. 20世纪90年代,科学家发现并证明碳有新的单质形态C60存在。后来又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状分子,碳大大丰富了碳元素单质的家族。下列有关说法错误的是( )
20世纪90年代,科学家发现并证明碳有新的单质形态C60存在。后来又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状分子,碳大大丰富了碳元素单质的家族。下列有关说法错误的是( )
A.熔点比较:C90<金刚石
B.金刚石与C70 管状碳和洋葱状碳都是石墨的同素异形体
C.已知C(石墨,s)= C(金刚石,s);△H>0,则石墨比金刚石稳定
D.C60晶体如图,每个C60分子周围与它距离最近且等距离的C60分子有10个
第Ⅱ卷 非选择题 共4小题,共50分
24.根据下表给出的数据判断,下列说法中肯定错误的是( )
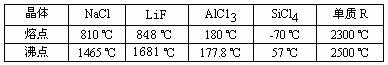
A.SiCl4是分子晶体 B.LiF中键的强度比NaCl中键的强度小
C.单质R是原子晶体 D.AlCl3为分子晶体
23.将某溶液逐滴加入Al (OH)3胶体内,开始产生沉淀,继续滴加沉淀又溶解,该溶液不可能是 ( )
A.2 mol·L-1H2SO4溶液 B.2 mol·L-1NaOH溶液
C.2 mol·L-1氨水溶液 D.2 mol·L-1Ba(OH)2溶液
22.能用渗析分离方法提纯的物质组是( )
A.蔗糖中混有少量NaCl杂质 B.碘中混有少量NaCl
C.蛋白质与葡萄糖的混合溶液 D.硫酸铜和明矾的混合溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com