
题目列表(包括答案和解析)
10.可逆反应2NO2(g)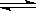 2NO(g)+O2(g)在恒容密闭容器中反应,可以作为达到平衡状态的标志是( )
2NO(g)+O2(g)在恒容密闭容器中反应,可以作为达到平衡状态的标志是( )
①单位时问内生成n mo1 O2的同时生成2nmol NO2
②单位时间内生成nmol O2的同时生成2nmolNO(g)
③混合气体的颜色不再改变
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
A.①③⑤ B.②④⑤ C.①③④ D.①②③④⑤
9.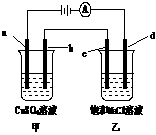 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
A.甲、乙两烧杯中溶液的pH均保持不变
B.甲烧杯中a的电极反应式为4OH――4e-=O2↑+2H2O
C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀
D.当b极增重3.2g时,d极产生的气体为2.24L(标准状况)
8.现有浓度为1 mol/L的五种溶液:①HCI,②H2SO4,③CH3COOH,④NaOH,由水电离出的C(H+)大小关系正确的是( )
A.③>①=④>② B.①=②>③>④ C.②>①>③>④ D.③>①>④>②
7.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq)
C.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
D.电池工作时,电子由正极通过外电路流向负极
6.已知:CH3CH2CH2CH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH =-2878 kJ/mol
4CO2(g)+5H2O(l);DH =-2878 kJ/mol
(CH3)2CHCH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH =-2869 kJ/mol
4CO2(g)+5H2O(l);DH =-2869 kJ/mol
下列说法正确的是( )
A.正丁烷分子储存的能量大于异丁烷分子 B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程 D.异丁烷分子中的碳氢键比正丁烷的多
5.在N2+3H2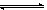 2NH3的反应中,经过一段时间内,NH3的浓度增加了0.6 mol·L-1,在此段时间内用H2表示的平均反应速率为0.45 mol·L-1·s-1,则所经过的时间是( )
2NH3的反应中,经过一段时间内,NH3的浓度增加了0.6 mol·L-1,在此段时间内用H2表示的平均反应速率为0.45 mol·L-1·s-1,则所经过的时间是( )
A.1 s B.2 s C.0.44 s D.1.33 s
4.某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的量浓度分别为c(X2)=0.4 mol/L,c(Y2)=0.8 mol/L,c(Z)=0.4 mol/L,则反应式可表示为( )
A.X2+2Y2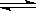 2XY2 B.2X2+Y2
2XY2 B.2X2+Y2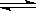 2X2Y
2X2Y
C.3X2+Y2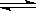 2X3Y D.X2+3Y2
2X3Y D.X2+3Y2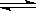 2XY3
2XY3
3.下列关于催化剂的说法,正确的是( )
A.催化剂能使不起反应的物质发生反应 B.催化剂在化学反应前后,性质和质量都不变
C.催化剂能改变化学反应速率 D.任何化学反应,都需要催化剂
2.下列叙述正确的是( )
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
1.在2A+B==3C+4D反应中,下面表示的反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B.v (B)=0.4 mol·L-1·s-1
C.v (C)=0.9 mol·L-1·s-1 D.v (D)=1.0 mol·L-1·s-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com