
题目列表(包括答案和解析)
8.2009年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是( )
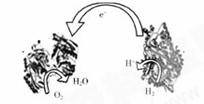
A.左边为该电池的正极 B.该电池可在高温环境下使用
C.该电池负极反应为:H2-2e-=2H+ D.该电池正极反应为O2+4e-=2O2-
7.已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和
-1366.8kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1 C.-330 kJ·mol-1 D.+330 kJ·mol-1
6. 在体积可变的容器中发生反应N2 + 3H2  NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是( )
NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是( )
A.分子运动速率加快,使反应物分子间的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D.分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
5.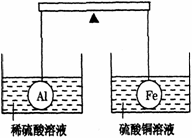 在杠杆的两端分别挂着质量和体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图,则下列说法正确的是( )
在杠杆的两端分别挂着质量和体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图,则下列说法正确的是( )
A.铝球一定是空心的
B.左边烧杯中的溶液质量减少了
C.去掉两烧杯杠杆仍平衡
D.右边铁球上出现红色
4.下列装置中能构成原电池的是( )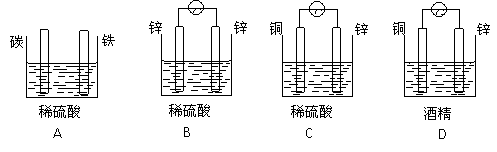
3.常温下,分别将四块形状相同、质量为9g的铁块同时投入下列四种溶液中,产生H2速率最快的是( )
A.200mL 2 mol·L-1HCl B.500mL 2 mol·L-1H2SO4
C.100mL 3 mol·L-1HCl D.500mL 6 mol·L-1 HNO3
2.下列有关化学方应方向的说法中正确的是( )
A.凡是焓变小于零的反应都能自发进行
B.凡是熵变小于零的化学反应都能自发进行
C.凡是焓变小于零,熵变大于零的化学变化都能自发进行
D.CaCO3在高温下的分解反应不属于自发过程
1.下列反应中生成物总能量高于反应物总能量的是 ( )
A.碳酸钙受热分解 B.乙醇燃烧 C.铝与稀硫酸反应 D.氧化钙溶于水
27、某烃在标准状况下的密度为 1.875g/L,其中含碳为85.7%,含氢为14.3%,这种烃能使溴水褪色。(1)该烃的分子式 ;
(2)写出其发生反应生成高聚物的化学方程式 。
26、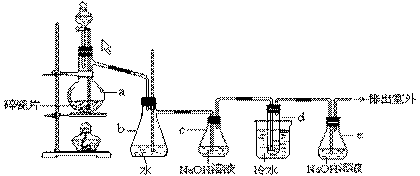 (7分)1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.___________ __________;________________________________;
(7分)1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.___________ __________;________________________________;
(2)瓶b的作用是___________________;
(3)容器c中NaOH溶液的作用是:__________________________________;
(4)瓶e的作用是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com