
题目列表(包括答案和解析)
28. (10分)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重 1.6 g。请回答下列问题
(10分)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重 1.6 g。请回答下列问题
(1)A接的是电源的 极。
(2)写出电解时B电极发生反应的电极反应式高*考*资*源*网
。
(3)反应的总离子方程式
。
(4)电解后溶液中氢离子的浓度为 ;要使电解后溶液恢复到电解前的状态,则可加入 , [ 填NaOH或CuO或Cu(OH)2 ]
27.(10分)一定温度下,在容积为1L的密闭容器内放入2mol
N2O4和8 mol NO2,发生如下反应:2NO2(红棕色)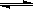 N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
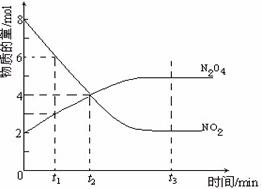 (1)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: mol·L-1·s-1
(1)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: mol·L-1·s-1
(2)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答: (3)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率
(4)维持容器的温度不变,若缩小容器的体积,则平衡向 移动 (填“正反应方向”、“逆反应方向”或“不移动”) 高*考*资*源*网
(5)维持容器的体积不变,升高温度,达到新平衡时体系的颜色 (填“变深”、“变浅”或“不变”)
26.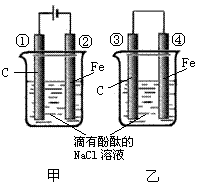 (10分)化学能和电能的相互转化,是能量转化的重要方式之一,右图两个实验装置是实现化学能和电能相互转化的装置。
(10分)化学能和电能的相互转化,是能量转化的重要方式之一,右图两个实验装置是实现化学能和电能相互转化的装置。
(1)把化学能转化为电能的装置是 (填“甲”或“乙”)
(2)④电极上的电极反应式为
(3)①电极上的电极反应式为
检验该电极反应产物的方法是
(4)甲、乙两装置电极附近的溶液首先变红的电极分别是 、 (填序号)高*考*资*源*网
(5)写出装置甲的反应总方程式
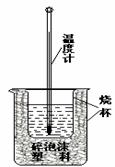
25.(5分)实验室利用如右图装置进行中和热的测定。高*考*资*源*网
 回答下列问题:
回答下列问题:
①该图中有两处未画出,它们是 、 ;
②在操作正确的前提下提高中和热测定的准确性的关键是 ;
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将 (填“偏大”、“偏小”、“不变”);原因是 。
24. 在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 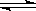 2SO3(g);(正反应放热),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是 ( )
2SO3(g);(正反应放热),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是 ( )
A.图I研究的是t0时刻增大O2的物质的量浓度对反应速率的影响
B.图II研究的是t0时刻通入氦气增大体系压强对反应速率的影响
C.图III研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较高
第Ⅱ卷
(本卷包括6小题,共52分)
23.在密闭容器中下列反应达平衡时,若降低温度可使混合气体平均相对分子质量减小的 是 ( )A.4NH3(g)+5O2(g)

 4NO(g)+6H2O(g) ;△H<0
4NO(g)+6H2O(g) ;△H<0
B.N2(g)+3H2(g)

 2NH3(g) ;△H<0
2NH3(g) ;△H<0
C.2SO3(g) 
 2SO2(g)+O2(g)
;△H>0
2SO2(g)+O2(g)
;△H>0
D.H2(g)+I2(g) 
 2HI(g) ;△H<0
2HI(g) ;△H<0
22.
 右图表示反应X(g)
右图表示反应X(g) 4Y(g)+Z(g),ΔH<0,在某温度时
4Y(g)+Z(g),ΔH<0,在某温度时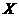 的浓度随时间变化的曲线:
的浓度随时间变化的曲线:
下列有关该反应的描述正确的是( )
A.第6 后,反应就终止了
后,反应就终止了
B.X在第一分钟和第二分钟内的
平均反应速率之比是3:2
C.该反应的过程是熵减小的过程
D.若降低温度,v正减少v逆增大。高*考*资*源*网
21.用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.1 mol·L-1 B.2 mol·L-1 C.3 mol·L-1 D.4 mol·L-1
20.T ℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
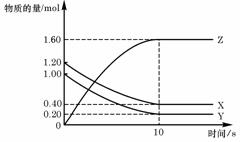
下列描述正确的是( )
A.平衡时X、Y的转化率相同
B.达到平衡后,将容器体积压缩为1 L,平衡向正反应方向移动
C.T ℃时,该反应的化学方程式为:X(g)+Y(g) 2Z
(g),平衡常数K= 40
2Z
(g),平衡常数K= 40
D.T ℃时,若起始时X为0.71 mol,Y为1.00 mol,则平衡时Y的转化率为60%
19.对于热化学方程式:SO3(g)
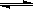 SO2(g)+
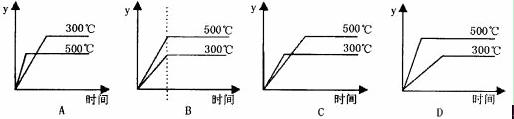
1/2 O2(g) ;△H=+ 98.3kJ•mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)( )
SO2(g)+
1/2 O2(g) ;△H=+ 98.3kJ•mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com