
题目列表(包括答案和解析)
18.25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是( )
H++OH-;ΔH>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
17.在相同温度下,等体积、等物质的量浓度的下列溶液①Na2SO4、②H2SO3、③NaHSO3、④Na2S中,所含带电微粒数由多到少的顺序为( )
A ④>①>③>② B ①>④>③>②
C ①=④>②=③ D ④=①>③>②
16.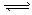 已知H2(g)+I2(g) ) 2HI(g)
已知H2(g)+I2(g) ) 2HI(g) 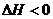 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol ,
有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol ,
乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的
措施是( )
A.甲、乙提高相同温度 B.甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D.甲增加0.1mol H2,乙增加0.1mol I2
14.在下列溶液中,各组离子一定能够大量共存的是( )
A、使酚酞试液变红的溶液: Na+、Cl-、SO42-、Fe3+
B、由水电离的c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
C、在pH = 1溶液中:NH4+、Fe2+、NO3-、Cl-
D、所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ 15.已知:为使Fe3+、Fe2+、Zn2+较完全的形成氢氧化物沉淀,溶液的pH应分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量Fe3+、Fe2+,为除去这些离子制得纯净的硫酸锌,应加入的试剂是( )
A.NaOH溶液 B.氨水 C.KMnO4、ZnCO3 D.H2O2、ZnO
13.关于小苏打水溶液的表述正确的是( )
A、c (Na+)=c
(HCO3-) + c (CO32-) + 2c (H2CO3)
B、c (Na+)
+ c (H+) = c (HCO3-) + 2c (CO32-) +c (OH-)
C、HCO3- 的电离程度大于HCO3-的水解程度
D、存在的电离有:NaHCO3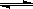 Na++HCO3-,HCO3-
Na++HCO3-,HCO3- 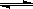 H++CO32-,H2O
H++CO32-,H2O 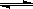 H++OH-
H++OH-
12.相同温度下,100mL 0.01 mol·L-1的醋酸溶液与10mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
A.中和时所需NaOH的量 B.c(H+)
C.c(OH-) D.c(CH3COOH)
11.常温下,取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的PH等于12,则原溶液的浓度为( )
A.0.01mol/L B. 0.017mol/L C. 0.05mol/L D. 0.50mol/L
10.某温度下,已知反应mX(g)+ nY(g)  qZ(g) △H>0,m + n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是( )
qZ(g) △H>0,m + n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是( )
A.反应速率υ正(X) =(n/m)υ逆(Y) B.加入X,反应的△H增大
C.增加Y的物质的量,X的转化率增大 D.降低温度,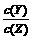 的值变小
的值变小
9.在恒温恒压的密闭容器中,充入 4L X和3L Y的混合气体,在一定条件下发生下列反应:
 4X(g)+3Y(g) 2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是 ( )
4X(g)+3Y(g) 2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是 ( )
A.8 B.6 C.5 D.3
8.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是( )
|
实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
|
V/mL |
c/(mol·L-1) |
V/mL |
c/(mol·L-1) |
V/mL |
||
|
A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com