
题目列表(包括答案和解析)
31.(9分)常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1︰2的体积比混合,所得溶液的pH=12。用上述NaOH溶液滴定pH=3的某一元弱酸溶液20ml,达到终点时消耗NaOH溶液13ml,试求:
(1)NaOH溶液的物质的量浓度
(2)此一元弱酸的物质的量浓度
(3)求此条件下该一元弱酸的电离平衡常数
30.(4分)用标准的NaOH溶液滴定未知浓度的盐酸(盛于锥形瓶中),造成测定结果偏高的原因可能是 。
A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.未用标准液润洗碱式滴定管
29.(15分)用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品,所用的仪器是 、 、 。
(2)将样品配成250mL待测液,还需的仪器有 、 、 。
(3)取10.00mL待测液,用 量取。
(4)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,选用酚酞为指示剂,滴定时 手旋转酸式滴定管的玻璃活塞, 手不停地摇动锥形瓶,两眼注视 ,直到滴入一滴标准盐酸时溶液立即由 色变成 色,且 ,则达到滴定终点。
(5)根据下列数据,计算待测烧碱溶液的物质的量浓度: 。
|
滴定次数 |
待测液体积 (mL) |
标准盐酸体积(mL) |
|
|
滴定前读数(mL) |
滴定后读数(mL) |
||
|
第一次 |
10.00 |
0.50 |
20.40 |
|
第二次 |
10.00 |
4.00 |
24.10 |
28.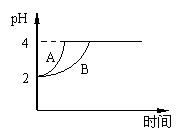 (4分)常温下,取pH=2的盐酸和醋酸溶液各100mL,
(4分)常温下,取pH=2的盐酸和醋酸溶液各100mL,
向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化
如右图所示。则图中表示醋酸溶液中pH变化曲线的是
(填“A”或“B”)。设盐酸中加入的Zn质量为m1, 醋酸溶液
中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)
27.(5分)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。则该溶液呈 性。在分析该溶液遇酚酞呈红色原因时,甲同学认为盐溶液应呈中性,所以可能是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
。
26.(7分)常温下将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L溶液。
(1)溶液中共有 种不同粒子。
(2)这些粒子中浓度为0.01 mol·L-1的是 ,浓度为0.002 mol·L-1的是 。
(3)物质的量之和为0.01mol的两种粒子是 和 。
(4) 和 两种离子数量之和比OH-多0.008mo1。
25.(2分)下列说法中不正确的是 。
①用稀HCl洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②一般地,物质的溶解度随温度的升高而增加,故物质的溶解大多是吸热的;
③除去溶液中的Mg2+,用OH-沉淀比用CO32-好,说明Mg(OH)2的溶解度比MgCO3大;
④沉淀反应中常加过量的沉淀剂,其目的是使沉淀更完全。
24.(8分)(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸”、“中”或“碱”,下同),溶液中c(Na+) c(CH3COO-)(填“>”、“=”或“<”,下同)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,溶液中
c(Na+) c(CH3COO-)
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,醋酸体积 氢氧化钠溶液体积。
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
23.常温下设a代表Ba(OH)2,b代表NaOH溶液,c代表NH3·H2O溶液。下列说法正确的是
A.同物质的量浓度的三种溶液的pH:a>b>c
B.同pH时,三种溶液稀释相同倍数后,pH:c>a>b
C.同pH、同体积的三种溶液消耗同浓度盐酸 的体积:a=b=c
D.同pH时,稀释不同倍数、pH仍相同,三种溶液稀释的倍数:a>b>c
22.下列叙述正确的是
A.浓度均为0.1mol·L-1的小苏打溶液与烧碱溶液等体积混合:
c(Na+)+c(H+) = 2c(CO32-)+c(OH-)
B.某二元酸(用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA-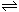 H++A2-则NaHA溶液中:c(Na+) = c(A2-)+c(HA-)+c(H2A)
H++A2-则NaHA溶液中:c(Na+) = c(A2-)+c(HA-)+c(H2A)
C.pH=12的氨水溶液与pH=2的盐酸溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.常温下,10 mL pH=12的Ba(OH)2溶液与40 mLcmol·L-1的NaHSO4溶液混合,当溶液中的Ba2+、SO42-均恰好完全沉淀,若混合后溶液的体积为50 mL,则溶液pH=11
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com